题目内容
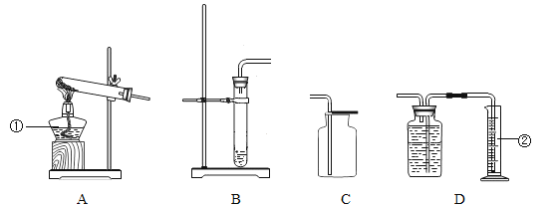
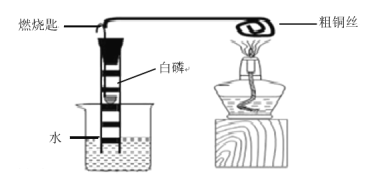
【题目】依据下图所示实验回答问题。
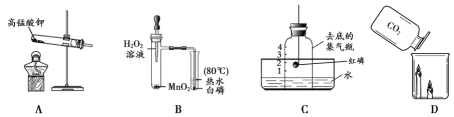
(1)A 中发生反应的化学方程式为__________。
(2)B用来探究燃烧的条件,由此得出燃烧的结论是__________。
(3)C中能证明空气中氧气含量的现象是__________。
(4)D中观察到的现象是________。
【答案】2KMnO4![]() K2MnO4+MnO2+O2↑ 可燃物燃烧需要与氧气接触 集气瓶内水面升至“1”处 蜡烛从上到下依次熄灭
K2MnO4+MnO2+O2↑ 可燃物燃烧需要与氧气接触 集气瓶内水面升至“1”处 蜡烛从上到下依次熄灭
【解析】
(1)A 中发生的是高锰酸钾受热生成锰酸钾、二氧化锰、氧气,反应的化学方程式为2KMnO4![]() K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
(2)B用来探究燃烧的条件,由此得出燃烧的结论是可燃物燃烧需要与氧气接触。
(3)C中红磷燃烧消耗氧气,氧气约占空气体积的五分之一,反应后集气瓶内压强减小,水面上升,能证明空气中氧气含量的现象是集气瓶内水面升至“1”处。
(4)二氧化碳不可燃不助燃且密度比空气大,D中观察到的现象是蜡烛从上到下依次熄灭。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案【题目】为了研究物质的溶解现象,进行如下探究活动。
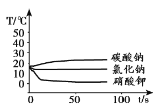
探究I:将足量的碳酸钠、氯化钠和硝酸钾三种物质分别溶解在一定量的水中,溶解过程的温度变化如下图所示。
探究II:
实验 |
① |
② |
③ |
现象 | 固体溶解, 形成紫红色溶液 | 固体溶解,形成紫红色溶液 | 固体几乎不溶解 |
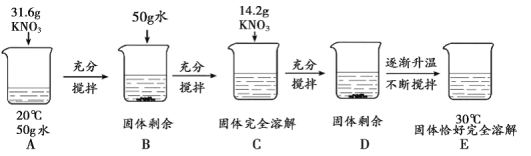
探究III: 探究过程如下图所示:
回答下列问题:
(1)探究I中,溶解过程放出热量的物质是__________。
(2)对探究II中实验现象进行分析,需要做的对比是________。分析得出的结论之一是__________。
(3)探究III中,所得溶液一定属于饱和溶液的是__________。通过该探究得出的结论是__________(答一点即可)。
(4)在上述探究的基础上,同学们想通过探究,比较食盐和氯化铵在水中的溶解度大小,探究方案应该是__________。