题目内容
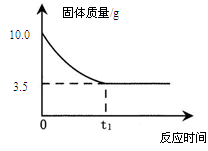
如下图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表。

(l)反应中二氧化锰的作用是 。
(2)反应生成氧气的质量为 g(结果精确到0. 1 g,下同)。
(3)计算参加反应的过氧化氢的质量,写出必要的计算过程。

| | 气体发生装置内物质的总质量 |
| 反应前 | 35.6 |
| 反应后 | 34.8 |
(l)反应中二氧化锰的作用是 。
(2)反应生成氧气的质量为 g(结果精确到0. 1 g,下同)。
(3)计算参加反应的过氧化氢的质量,写出必要的计算过程。
(1)加快过氧化氢分解的速率
(2)0.8
(3)1.7g
(2)0.8
(3)1.7g
(1)二氧化锰是催化剂,它能加快过氧化氢分解的速率。
(2)根据质量守恒定律,反应生成氧气的质量=35.6g-34.8g=0.8g。
(3)根据方程式中过氧化氢与氧气的质量关系,由0.8g氧气可求出参加反应的过氧化氢的质量,这属于简单的化学方程式的计算。解题时要规范解题格式、步骤。
(3)解:设参加反应的过氧化氢的质量为x
2H2O2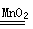 2H2O + O2↑
2H2O + O2↑
68 32
x 0.8g
68∶x = 32∶0.8g
x=1.7g
答:参加反应的过氧化氢的质量为1.7g。
(2)根据质量守恒定律,反应生成氧气的质量=35.6g-34.8g=0.8g。
(3)根据方程式中过氧化氢与氧气的质量关系,由0.8g氧气可求出参加反应的过氧化氢的质量,这属于简单的化学方程式的计算。解题时要规范解题格式、步骤。
(3)解:设参加反应的过氧化氢的质量为x
2H2O2
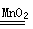 2H2O + O2↑
2H2O + O2↑68 32
x 0.8g
68∶x = 32∶0.8g
x=1.7g
答:参加反应的过氧化氢的质量为1.7g。

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目