题目内容
(现有硫酸铜、氯化钠、氢氧化钠、硫酸钠四种溶液,通过观察即可鉴别出来的是 _________ (填化学式,下同)溶液,将其滴加到另外三种溶液中可鉴别出 _________ 溶液,写出该反应的化学方程式 _________ .剩余的两种溶液,各取少量原溶液再滴加 _________ 溶液即可进行鉴别.
CuSO4、NaOH CuSO4+2NaOH==Cu(OH)2↓+Na2SO4 BaCl2或Ba(NO3)2
解析试题分析:通过观察,有特殊颜色的溶液先鉴别出来,硫酸铜溶液是蓝色,然后利用硫酸铜溶液跟剩下的三种溶液反应,其中氢氧化钠能与硫酸铜溶液反应,生成氢氧化铜蓝色沉淀,反应的化学方程式:CuSO4+2NaOH==Cu(OH)2↓+Na2SO4,氯化钠和硫酸钠2种溶液,可用BaCl2或Ba(NO3)2溶液进行鉴别,能与BaCl2或Ba(NO3)2溶液反应生成白色沉淀的是硫酸钠溶液
考点:特征颜色的溶液,SO42-的检验

 名校课堂系列答案
名校课堂系列答案(4分)请从下列六种物质中,选择相应物质的序号字母填空:
| A.氮气 | B.硫酸 | C.二氧化碳 | D.氢氧化钠 E.氢氧化钙 F.pH试纸 |
(3)可用于制肥皂、造纸等工业的碱 ; (4)用来降低土壤酸性的物质____ __。
(6分)某化学兴趣小组查阅资料得知,粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。为了将粗盐提纯,设计了以下操作流程: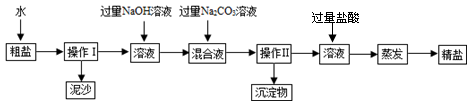
请你根据以上信息回答下述问题:
(1)操作Ⅰ的名称为_______________。
(2)加入过量氢氧化钠溶液,发生化学反应的方程式为 。
(3)加入过量碳酸钠溶液的实验目的是 。
经过操作Ⅱ所得溶液中含有的阴离子是 。
过滤
(4)某同学所得精盐比其他同学明显要多,原因可能是__________。AB
_______ ____
| A.滤纸破损,滤液浑浊就蒸发 |
| B.蒸发时未用玻璃棒,有一些液体溅出 |
| C.提纯后所得精盐尚未完全干燥 |
| D.溶解时水的量太少,使食盐未完全溶解 |
将X溶液逐滴滴入Y溶液中,在滴加过程中,Y溶液的pH变化情况如图所示。
| 溶液 | A组 | B组 | C组 | D组 |
| X | 盐酸 | 盐酸 | 氢氧化钙 | 氢氧化钙 |
| Y | 氢氧化钙 | 水 | 盐酸 | 水 |
(1)表格中符合这种变化情况的是 组(填写编号),理由是
(2)处于图中m点时,溶液中的溶质为 。