题目内容
(4分)某环保小组监测到一工厂排放的废水中含有H2SO4和CuSO4 。为了测定废水中CuSO4的质量分数,该小组取了100g废水,逐滴加入10%的NaOH溶液至过量。测得生成Cu(OH)2沉淀质量与所加NaOH溶液质量关系如下图所示。
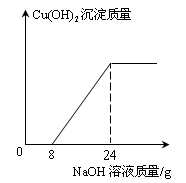
(1)与H2SO4反应的NaOH溶液质量为 g;100g废水中H2SO4的质量为 g。
(2)计算废水中CuSO4的质量分数。

(1)与H2SO4反应的NaOH溶液质量为 g;100g废水中H2SO4的质量为 g。
(2)计算废水中CuSO4的质量分数。
(1) 8 0.98 (2)3.2%
(1)H2SO4和CuSO4都与NaOH反应,但酸碱中和反应优先,由图示可知与H2SO4反应的NaOH溶液质量为8g。设100g废水中H2SO4的质量为x
H2SO4 + 2NaOH ="=" Na2SO4 + 2H2O
98 80
x 8g×10%
98:80=x:8g×10% 解得 x=0.98g
(2)设废水中CuSO4的质量分数为y
CuSO4 + 2NaOH ="=" Na2SO4 + Cu(OH)2↓
160 80
100×y (24-8)g×10%
160: 80="(100×y):[" (24-8)g×10%] 解得 y=3.2%
答:废水中CuSO4的质量分数为3.2%。
H2SO4 + 2NaOH ="=" Na2SO4 + 2H2O
98 80
x 8g×10%
98:80=x:8g×10% 解得 x=0.98g
(2)设废水中CuSO4的质量分数为y
CuSO4 + 2NaOH ="=" Na2SO4 + Cu(OH)2↓
160 80
100×y (24-8)g×10%
160: 80="(100×y):[" (24-8)g×10%] 解得 y=3.2%
答:废水中CuSO4的质量分数为3.2%。

练习册系列答案
相关题目