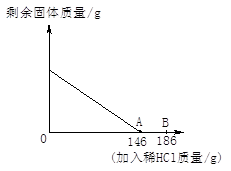题目内容
现有4.9gMgO、Mg(OH)2的固体混合物,与100g9.8%的稀H2SO4恰好完全反应,形成不饱和溶液。则原固体混合物中镁元素的质量为
| A.1.2g | B.1.6g | C.2.4g | D.4.8g |
C
MgO、Mg(OH)2与H2SO4反应化学方程式:MgO+H2SO4==MgSO4+H2O、Mg(OH)2+H2SO4== MgSO4+2H2O 由以上两个化学方程式和质量守恒定律可知,
Mg ~ MgSO4 ~ H2SO4
24 98
x 100g×9.8%
24:98=x:100×9.8% 解得 x="2.4g"
故选C
Mg ~ MgSO4 ~ H2SO4
24 98
x 100g×9.8%
24:98=x:100×9.8% 解得 x="2.4g"
故选C

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目