题目内容
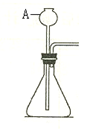
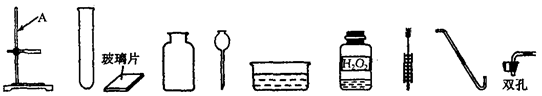
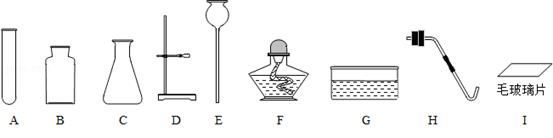
实验室制取气体的装置如图所示,根据所学的知识回答下列问题。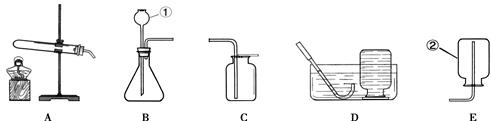
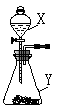
(1)图中标有②的仪器名称是 。
(2)写出用装置A制氧气的一个化学方程式 。
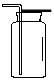
(3)写出用石灰石和稀盐酸制取二氧化碳,可选用图中 和 (填序号)组装一套制取二氧化碳的装置。用澄清石灰水检验二氧化碳的化学方程式为 。
(1)集气瓶(2)2KMnO4 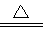 K2MnO4 + MnO2 + O2↑ (或2KClO3
K2MnO4 + MnO2 + O2↑ (或2KClO3  2KCl + 3O2↑ (3)B C Ca(OH)2 + CO2
2KCl + 3O2↑ (3)B C Ca(OH)2 + CO2 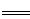 CaCO3 ↓+ H2O
CaCO3 ↓+ H2O
解析试题分析:(2)A装置属固固加热型,故可用高锰酸钾或氯酸钾制取氧气;
(3)根据反应物的状态和反应条件选择发生装置,用用石灰石和稀盐酸制取二氧化碳,,属于固液体常温下的反应,故选B作为发生装置;二氧化碳的密度比空气答,可用C装置收集;二氧化碳用澄清的石灰水检验。
考点:常用气体的发生装置和收集装置与选取方法

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案如图是实验室常用的气体制备、收集的多种功能装置。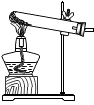
A B C D E F
(1)若实验室用A装置加热氯酸钾和二氧化锰混合物制取氧气,其化学方程式为 。
(2)若B装置X中盛放稀盐酸、Y中盛放石灰石,B与C组成发生、收集CO2气体的系列装置,检验CO2收满的方法是 ,检验制得气体是否为二氧化碳的化学方程式为 。
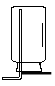
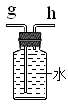
(3)若实验室用锌粒和稀硫酸制取氢气,可选择的发生装置为 ,反应的化学方程式为 。若用排水法收集并测定氢气的体积,氢气从E装置导管口 (填“g”或“h”) 进。选用仪器F测量排出水的体积,仪器F的名称是 。
(4)对锌与稀硫酸反应快慢的影响因素进行探究。反应过程中,利用前10min 内收集的氢气体积比较反应的快慢。控制其他条件相同,进行下表四组实验,获得数据如下:
| 实验编号 | 试剂 | 前 10 min 内产生的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和溶质质量分数的稀硫酸 | ||
| a | 纯锌 | 30mL 30% | 564.3 |
| b | 含杂质的锌 | 30mL 30% | 634.7 |
| c | 纯锌 | 30mL 20% | 449.3 |
| d | 纯锌 | 40mL 30% | 602.8 |
Ⅰ. 比较实验a和实验b,可以得到的结论是 。
Ⅱ.要比较不同溶质质量分数的硫酸对反应快慢的影响,应选择的实验编号是 。
Ⅲ. 控制其他条件相同,还需考虑控制的条件是 (例举一种条件即可)。
相关资料:
(一)盐酸是一种挥发性的酸,它会发出的氯化氢气体是一种易溶于水的气体.氯化氢溶于水既得盐酸;盐酸的挥发性随其溶质的质量分数减小而减弱.盐酸和醋酸一样能使紫色的石蕊试液变成红色.
(二)硫酸钙微溶于水.石灰石与稀硫酸反应,生成的硫酸钙会覆盖在石灰石表面,阻碍反应的继续发生.
请你和小明仪器进行实验室制取二氧化碳的探究.
(1)选择药品.小明对三组药品进行了实验研究,实验记录如下:
| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钙粉末和稀盐酸 | 产生气泡速率很快 |
从制取和收集的角度分析,一般选择第①组药品,该组药品发生反应的化学方程式为 _________ ;不选择第③组药品的原因是 _________ .
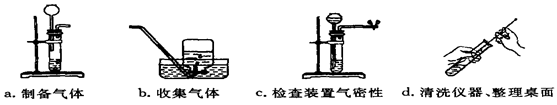
(2)选择装置.通过对制取氧气装置的分析,他选择用过氧化氢制取氧气的发生装置.你认为他选择的依据是 _________ .
(3)制取气体.将药品装入所选装置制取气体,并用向上排空气法收集.验满方法是 _________ .
(4)气体检验.将生成的气体通入石蕊溶液中,溶液变红,因此他确定该气体是二氧化碳.他的检验方法是否正确?请说明理由. _________ .


 NH3↑+HCl↑
NH3↑+HCl↑
