题目内容
【题目】在宏观、微观和符号之间建立联系是化学特有的思维方式。
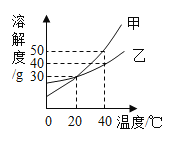
(1)在氧气、铁和氯化钠三种物质中,保持氧气化学性质的最小粒子是___________;由离子构成的物质是__________________。
(2)某化学反应的微观示意图如下:
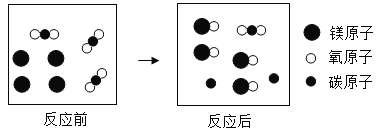
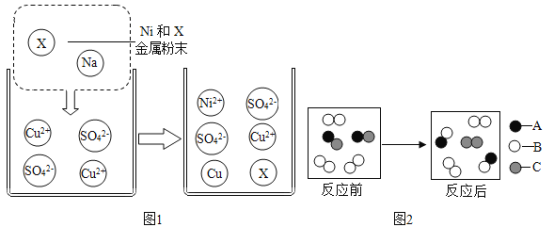
①反应涉及到的物质中,![]() 是由___________(填“分子”、“原子”或“离子”)构或的单质,有____________种氧化物.
是由___________(填“分子”、“原子”或“离子”)构或的单质,有____________种氧化物.
②参加反应的![]() 和
和![]() 的微粒个数比是____________(写出最简整数比)
的微粒个数比是____________(写出最简整数比)
③反应生成的单质和化合物的质量比是_______________
【答案】氧气分子 氯化钠 原子 2 1:2 3:20
【解析】
(1)氧气是由氧气分子构成的,铁是由铁原子构成的,氯化钠是由氯离子和钠离子构成的,氧气是由氧气分子构成的,所以保持氧气化学性质的最小粒子是氧气分子;由粒子构成的是氯化钠;
(2)①由微观示意图可知,![]() 表示镁原子,是由原子构成的单质,图中共有2中氧化物,分别为MgO,CO2;
表示镁原子,是由原子构成的单质,图中共有2中氧化物,分别为MgO,CO2;
②由微观示意图可知,反应的方程式为2Mg+CO2![]() 2MgO+ C,
2MgO+ C, ![]() 表示Mg,
表示Mg,![]() 表示CO2,所以微粒个数比为2:1;
表示CO2,所以微粒个数比为2:1;
③
所以生成的单质和化合物的质量比为12:80=3:20.

 全能测控期末小状元系列答案
全能测控期末小状元系列答案【题目】某化学兴趣小组在一次实验活动中发现镁、钠都能在纯净的二氧化碳气体中燃烧,反应后冷却,瓶底除了有黑色颗粒,瓶壁上还都附着白色物质。经检验,黑色颗粒是碳。他们对镁、钠在二氧化碳气体中燃烧后生成的白色物质分别进行了如下探究:
(探究问题一)镁在纯净的二氧化碳中燃烧生成的白色物质是什么?
同学们首先排除了是Mg(OH)2的可能性,理由是_____。
(做出猜想)白色固体可能是①MgO、②MgCO3、③_____。
(进行实验)取少量白色固体,加入足量的稀盐酸,观察到_____现象,猜想①正确。
(实验结论)镁在二氧化碳中燃烧的化学方程式是_____。
(探究问题二)钠在纯净的二氧化碳中燃烧生成的白色物质是什么?
(查阅资料)信息1:钠能与冷水发生剧烈反应。
信息2:Na2O+H2O=2NaOH
(实验设计)甲组方案:
实验步骤 | 实验现象 | 结论 |
取少量白色物质于试管中,加水溶解,加入足量Ba(OH)2溶液 | _____ | 白色物质中有Na2CO3 |
静置后,向上层清液滴加酚酞试液 | 溶液变红 | 白色物质中有Na2O |
甲组结论:白色固体为Na2O和Na2CO3的混合物
乙组方案:
取5.3克白色固体样品进行下列操作:
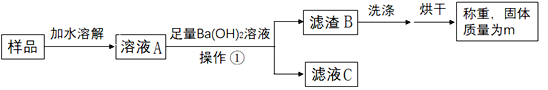
(1)操作①是_____。
(2)Ba(OH)2溶液必须足量的目的是_____。
该组同学测得m=9.85克,结合样品质量进行分析,最终得出结论:白色固体为Na2CO3。
(实验反思)
(1)为何甲、乙两组所得结论不相符,某同学分析后指出甲组方案不科学,应该将甲组方案中的Ba(OH)2溶液改为_____溶液才合理。
(2)钠在二氧化碳中燃烧的化学方程式为_____。
(拓展应用)
实验室里钠等金属因燃烧引发火灾时,可以选择的灭火方式有_____。
A 用水浇灭 B 用液态二氧化碳灭火器 C 撒沙土盖灭
【题目】某校兴趣小组的同学为了测定某石灰石中碳酸钙的质量分数,他们取该石灰石样品10g加入烧杯中,再把80g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的杂质既不溶于水,也不与稀盐酸反应):
实验次数 | 第 1 次 | 第 2 次 | 第 3 次 | 第 4 次 |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 |
剩余固体的质量/g | 6 | m | 1.2 | 1.2 |
分析表中数据,完成下列问题:
(1)表中m的数值为___;
(2)计算稀盐酸的溶质质量分数____。