题目内容
【题目】铬(Cr)是重要的金属材料,越来越受到人们的关注。某化学兴趣小组对Cr、Al、Cu的金属活动性顺序进行探究,过程如下:
(提出假设)
(1)由已学知识,已知其中两种金属的活动性顺序,现对三种金属的活动性顺序提出三种可能的假设:
a.Al>Cr>Cu b.Cr>Al>Cu c._____。
(设计实验)同温下,取大小相同的打磨过的金属薄片,分别投入到等体积等浓度的足量稀盐酸中,观察现象,记录如下:
金属 | Cr | Al | Cu |
与盐酸 反应现象 | 气泡产生缓慢, 金属逐渐溶解 | 气泡产生剧烈, 金属迅速溶解 | 无气泡产生, 金属无变化 |
(控制实验条件)
(2)打磨三种金属目的是除去表面氧化膜,其发生的是___变化(填“物理”或化学)
(得出结论)
(3)原假设中正确的是_____(填“a”“b”或“c”)。写出铬与盐酸反应的化学方程式(铬与盐酸反应后显+2价):_____。
(结论应用)
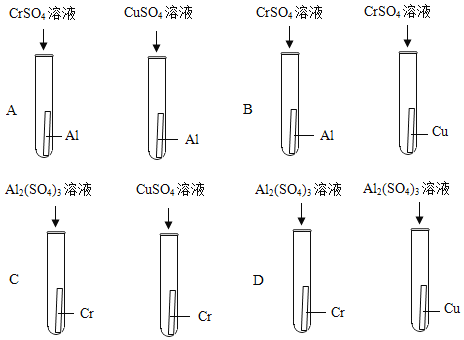
(4)根据探究结果,为验证Cr、Al、Cu的金属活动性顺序,还可设计如图所示的实验操作。其中可以达到实验目的是_____(填字母)。
【答案】Al>Cu>Cr 物理 a Cr+2HCl═CrCl2+H2↑ B、C
【解析】
(1)三种金属的活动性顺序可能是Al>Cr>Cu,也可能是Cr>Al>Cu,也可能是Al>Cu>Cr.故填:Al>Cu>Cr;
(2)打磨三种金属发生的是物理变化;故填:物理;
(3)铬与稀盐酸能够反应,说明比铜活泼,产生气泡不如铝和稀盐酸反应除去气泡剧烈,说明不如铝活泼,因此原假设中正确的是a;
铬与盐酸反应的化学方程式为:Cr+2HCl═CrCl2+H2↑.故填:a;Cr+2HCl═CrCl2+H2↑;
(4)铬和稀盐酸反应的速率比铝和稀盐酸反应的速率慢,说明铝比铬活泼,铜和稀盐酸混合无明显现象,说明铝和铬都比铜活泼,即三种金属的活动性:Al>Cr>Cu。
A.铝能置换出硫酸铬中的铬和硫酸铜中的铜,说明铝最活泼,但是无法证明Cr和Cu的活动性,不能验证三种金属的活动性;
B.铝能置换出硫酸铬中的铬,说明铝比铬活泼,铜不能置换出硫酸铬中的铬,说明铬比铜活泼,可以验证三种金属的活动性;
C.铬不能置换出硫酸铝中的铝,能置换出硫酸铜中的铜,说明铝的活动性大于铬,铬的活动性大于铜,可以验证三种金属的活动性;
D.铜和铬均不能置换出硫酸铝中的铝,说明铝最活泼,而无法验证铜和铬的活动性强弱,不能验证三种金属的活动性。
故填:B、C。

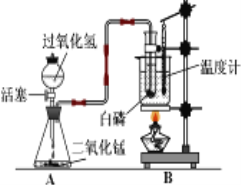
【题目】某校实验室有一瓶久置的铁屑,其成分是铁、氧化铁和水。为测定其中各成分的质量分数,某兴趣小组按下图所示装置进行实验(装置气密性良好;固定装置已略去;氮气不与铁屑中的成分反应;碱石灰是氧化钙和氢氧化钠的混合物)。
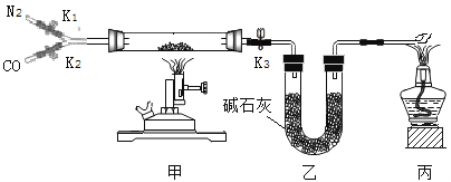
部分实验步骤如下:
Ⅰ.称量硬质玻璃管的质量。将样品放入硬质玻璃管中,称量硬质玻璃管和样品的质量。
II.连接好装置。缓缓通入N2,点燃甲处的酒精喷灯,待硬质玻璃管中固体恒重,记录硬质玻璃管和剩余固体的质量。
Ⅲ.再次连接好装置,继续实验。通入CO,点燃丙处的酒精灯和甲处的酒精喷灯。待硬质玻璃管中固体恒重,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却。再次记录硬质玻璃管和剩余固体的质量。
实验数据记录如下表:
硬质玻璃管 | 硬质玻璃管和样品 | 步骤II硬质玻璃 管和剩余固体 | 步骤步骤Ⅲ硬质玻璃 管和剩余固体 | |
质量 | m1 | m2 | m3 | m4 |
请回答下列问题:
(1)步骤Ⅲ丙处酒精灯的作用是____________。
(2)步骤Ⅲ硬质玻璃管中反应的化学方程式为________。
(3)样品中氧化铁的质量分数为_____(用m1、m2、m3、m4的代数式表示)。若步骤Ⅲ中氧化铁没有完全反应,样品中水的质量分数测量结果将______(填“偏大”“偏小”或“不变”)。
(4)有关样品,下列说法正确的是_____(填字母标号)。
A样品中氢元素的质量为1/9(m2-m3) B样品中铁单质和氧化铁的质量总和为m3-m1
C样品中铁单质的质量为m4-m1 D样品中氧元素的质量为m3-m4
【题目】通过一年的化学学习,同学们初步掌握了实验室制取气体的知识和技能,请完成下列
实验内容。
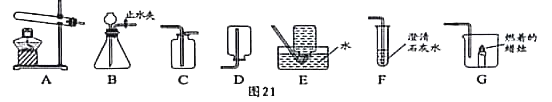
(制取气体)
实验名称 | 化学方程式 | 选用药品 | 制取气体所选装置 |
实验室制取二氧化碳 | ________ | 石灰石和稀盐酸 | BC |
实验室制取氧气 | ________ | _____ | _____ |
(探究活动)(1)通常将产生的二氧化碳通入装置F,目的是________.
(2)如果将产生的氧气通入装置G,现象是____________.
(交流总结)如果实验室需要制取另一种气体,你的思路是___________.(不写具体操作)。