题目内容
某化学兴趣小组对采集的石灰石样品进行了下列实验:取3份质量不同的石灰石样品,分别与30g相同溶质质量分数的稀盐酸充分反应后(石灰石样品中的杂质既不溶于水,也不与盐酸反应),经过滤、干燥,称量剩余固体的质量与所取样品质量的关系如下表所示:
试计算:
(1)石灰石样品中碳酸钙的质量分数;
(2)所用稀盐酸中溶质的质量分数.
| 实验序号 | 石灰石样品质量/g | 稀盐酸的质量/g | 剩余固体质量/g |
| 1 | 2.0 | 30.0 | 0.5 |
| 2 | 4.0 | 30.0 | 1.0 |
| 3 | 6.0 | 30.0 | 3.0 |
(1)石灰石样品中碳酸钙的质量分数;
(2)所用稀盐酸中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:由反应质量表可知,前两次实验中石灰石中碳酸钙完全反应,而第三次实验因盐酸量不足,石灰石中碳酸钙未能完全反应;2.0g石灰石完全反应剩余0.5g固体可知,2.0g该石灰石样品中含碳酸钙质量=2.0g-0.5g=1.5g,含杂质0.5g;
因此,第三次实验中参加反应的碳酸钙质量=6.0g-3.0g=3.0g;
计算所用稀盐酸中溶质质量分数时,应选取盐酸完全反应的第三次实验所记录数据进行,而前两次实验因盐酸未全部参加反应,不能用作计算稀盐酸的溶质质量分数.
因此,第三次实验中参加反应的碳酸钙质量=6.0g-3.0g=3.0g;
计算所用稀盐酸中溶质质量分数时,应选取盐酸完全反应的第三次实验所记录数据进行,而前两次实验因盐酸未全部参加反应,不能用作计算稀盐酸的溶质质量分数.
解答:解:(1)由碳酸钙完全反应的前两次实验数据可知:每2.0g该石灰石样品中含碳酸钙质量=2.0g-0.5g=1.5g,
该组样品中碳酸钙的质量分数=
×100%=75%;
(2)由第3次实验的数据得,消耗碳酸钙的质量=6.0g-3.0g=3.0g
设30.0g稀盐酸中HCl质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
3.0g x
=
x=2.19g
稀盐酸中溶质的质量分数=
×100%=7.3%
答:(1)石灰石样品中碳酸钙的质量分数为75%;
(2)所用稀盐酸中溶质的质量分数为7.3%.
该组样品中碳酸钙的质量分数=
| 1.5g |
| 2.0g |
(2)由第3次实验的数据得,消耗碳酸钙的质量=6.0g-3.0g=3.0g
设30.0g稀盐酸中HCl质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
3.0g x
| 100 |
| 3.0g |
| 73 |
| x |
x=2.19g
稀盐酸中溶质的质量分数=
| 2.19g |
| 30g |
答:(1)石灰石样品中碳酸钙的质量分数为75%;
(2)所用稀盐酸中溶质的质量分数为7.3%.
点评:第三次实验中所剩余的3.0gg固体为杂质及未反应完的碳酸钙的混合物,反应后前后质量差即为反应所消耗的碳酸钙质量.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
现有空气、氧气和二氧化碳三瓶气体,若一次性将它们区别出来,最简单的方法是( )
| A、看颜色、闻气味 |
| B、测密度 |
| C、分别插入燃着的木条 |
| D、分别倒入澄清石灰水 |
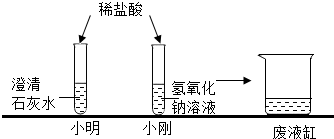 小明和小刚两位同学在学完酸的化学性质后,做了如图酸碱中和的反应实验:
小明和小刚两位同学在学完酸的化学性质后,做了如图酸碱中和的反应实验: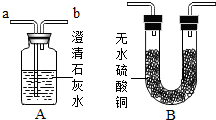 某学校化学课外活动小组,对铜制品生锈很感兴趣.经查阅资料,知道铜锈的主要成份是碱式碳酸铜,俗称铜绿,化学式为Cu2(OH)2CO3,他们在探究中发现,铜绿受热分解后,除生成二氧化碳和水蒸气外,试管中还有一些黑色粉末状固体,为了更清楚地了解这种黑色粉末,同学们准备通过实验探究,进一步分析黑色固体的组成,并验证产生的气体:
某学校化学课外活动小组,对铜制品生锈很感兴趣.经查阅资料,知道铜锈的主要成份是碱式碳酸铜,俗称铜绿,化学式为Cu2(OH)2CO3,他们在探究中发现,铜绿受热分解后,除生成二氧化碳和水蒸气外,试管中还有一些黑色粉末状固体,为了更清楚地了解这种黑色粉末,同学们准备通过实验探究,进一步分析黑色固体的组成,并验证产生的气体: