题目内容
某实验小组同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液加入稀盐酸一会后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:可能是CaCl2和Ca(OH)2;猜想二:可能只有CaCl2;
猜想三: .
【查阅资料】氯化钙溶液呈中性.
【进行实验】
实验步骤:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡
实验现象:
结论:猜想一不正确
实验步骤:取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量
实验现象: 结论:猜想二不正确,猜想三正确
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑 .
(2)根据所学化学知识,验证烧杯内溶液中的溶质含有HCl,除以上方案外,下列哪些物质单独使用也能完成该实验? (填序号)
a.pH试纸 b.铜 c.紫色石蕊溶液 d.硝酸银溶液
(3)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是 (写一条).
(4)要把该废液处理成只有一种溶质的溶液,应向该废液中加入过量的 反应结束后,过滤即可.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:可能是CaCl2和Ca(OH)2;猜想二:可能只有CaCl2;
猜想三:
【查阅资料】氯化钙溶液呈中性.
【进行实验】
实验步骤:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡
实验现象:
结论:猜想一不正确
实验步骤:取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量
实验现象:
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑
(2)根据所学化学知识,验证烧杯内溶液中的溶质含有HCl,除以上方案外,下列哪些物质单独使用也能完成该实验?
a.pH试纸 b.铜 c.紫色石蕊溶液 d.硝酸银溶液
(3)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是
(4)要把该废液处理成只有一种溶质的溶液,应向该废液中加入过量的
考点:实验探究物质的组成成分以及含量,酸的化学性质,碱的化学性质,中和反应及其应用
专题:科学探究
分析:【猜想】
烧杯内溶液中的溶质可能是CaCl2和Ca(OH)2,也可能只有CaCl2,也可能是CaCl2和HCl;
【进行实验】
显碱性的溶液能使酚酞试液变红色,显酸性或显中性的溶液不能使酚酞试液变色;
如果溶质是氯化钙和氯化氢,则逐滴加入碳酸钠溶液至过量时,碳酸钠先和稀盐酸反应生成氯化钠、水和二氧化碳,当稀盐酸完全反应后,碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠;
【反思与拓展】
在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否过量;
pH试纸、石蕊试液可以测定溶液的酸碱性;
显酸性的溶液能够腐蚀铁质下水管、水泥下水管等;
碳酸钙不溶于水,能和稀盐酸反应生成氯化钙、水和二氧化碳.
烧杯内溶液中的溶质可能是CaCl2和Ca(OH)2,也可能只有CaCl2,也可能是CaCl2和HCl;
【进行实验】
显碱性的溶液能使酚酞试液变红色,显酸性或显中性的溶液不能使酚酞试液变色;
如果溶质是氯化钙和氯化氢,则逐滴加入碳酸钠溶液至过量时,碳酸钠先和稀盐酸反应生成氯化钠、水和二氧化碳,当稀盐酸完全反应后,碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠;
【反思与拓展】
在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否过量;
pH试纸、石蕊试液可以测定溶液的酸碱性;
显酸性的溶液能够腐蚀铁质下水管、水泥下水管等;
碳酸钙不溶于水,能和稀盐酸反应生成氯化钙、水和二氧化碳.
解答:解:【猜想】
烧杯内溶液中的溶质可能是CaCl2和HCl.
故填:CaCl2和HCl.
【进行实验】
实验步骤:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡;
实验现象:酚酞试液不变色;
结论:猜想一不正确.
故填:酚酞试液不变色.
实验步骤:取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量;
实验现象:先产生气泡,后产生白色沉淀;
结论:猜想二不正确,猜想三正确.
故填:先产生气泡,后产生白色沉淀.
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否有剩余.
故填:反应物是否有剩余.
(2)如果烧杯内溶液中的溶质含有氯化氢,利用pH试纸测定溶液时,pH<7;
如果烧杯内溶液中的溶质含有氯化氢,滴加紫色石蕊溶液时,石蕊试液变红色.
故填:ac.
(3)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是腐蚀铁质下水管.
故填:腐蚀铁质下水管.
(4)要把该废液处理成只有一种溶质的溶液,应向该废液中加入过量的碳酸钙反应结束后,过滤即可.
故填:碳酸钙.
烧杯内溶液中的溶质可能是CaCl2和HCl.
故填:CaCl2和HCl.
【进行实验】
实验步骤:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡;
实验现象:酚酞试液不变色;
结论:猜想一不正确.
故填:酚酞试液不变色.
实验步骤:取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量;
实验现象:先产生气泡,后产生白色沉淀;
结论:猜想二不正确,猜想三正确.
故填:先产生气泡,后产生白色沉淀.
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否有剩余.
故填:反应物是否有剩余.
(2)如果烧杯内溶液中的溶质含有氯化氢,利用pH试纸测定溶液时,pH<7;
如果烧杯内溶液中的溶质含有氯化氢,滴加紫色石蕊溶液时,石蕊试液变红色.
故填:ac.
(3)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是腐蚀铁质下水管.
故填:腐蚀铁质下水管.
(4)要把该废液处理成只有一种溶质的溶液,应向该废液中加入过量的碳酸钙反应结束后,过滤即可.
故填:碳酸钙.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
化学实验是进行科学探究的重要途径.下列实验操作中,不符合操作规范的是( )
| A、实验室制取气体前要先检查装置的气密性 |
| B、测定溶液的酸碱度,将pH试纸直接伸入待测液中 |
| C、浓硫酸不慎沾到手上,立即用大量的水冲洗,然后涂上3%-5%碳酸氢钠溶液 |
| D、点燃氢气前,一定要先检验氢气的纯度 |
 现有A~F六种常见物质,其中A、B、C分属于酸碱盐中的一类物质,D是一种重要的温室气体,D、E、F都含有同种非金属元素,它们的关系如图,短线相连的物质间能反应,箭头表示物质间的转化关系.请回答:(1)写出D物质的化学式:
现有A~F六种常见物质,其中A、B、C分属于酸碱盐中的一类物质,D是一种重要的温室气体,D、E、F都含有同种非金属元素,它们的关系如图,短线相连的物质间能反应,箭头表示物质间的转化关系.请回答:(1)写出D物质的化学式:
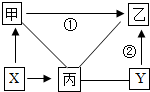 由C、H、O、Cu四种元素组成的初中常见物质,各物质之间有如图所示的关系,其中甲、乙、丙是单质,乙为紫红色固体,X、Y是氧化物.图中“-”表示相连的物质之间可发生反应,“→”表示由某一物质可制得另一物质.(反应条件已略去)请回答:
由C、H、O、Cu四种元素组成的初中常见物质,各物质之间有如图所示的关系,其中甲、乙、丙是单质,乙为紫红色固体,X、Y是氧化物.图中“-”表示相连的物质之间可发生反应,“→”表示由某一物质可制得另一物质.(反应条件已略去)请回答: