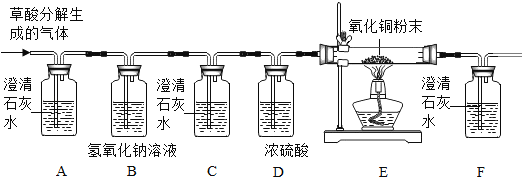
题目内容
【题目】如图是实验室中常见装置,回答下列问题:
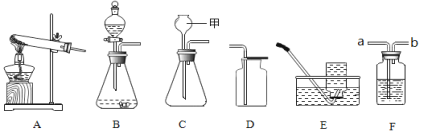
(1)C装置中,甲仪器的名称是______。
(2)实验室用双氧水和二氧化锰粉末制取氧气,发生装置常选用B而不选用C,其主要原因是______;若用E装置收集氧气,当___时,才开始收集。
(3)实验室可以按照“C→F→真空气囊”的装置顺序制取干燥的CO2气体,C装置中发生反应的化学方程式为_____,F装置应盛放的试剂为______(填名称),气体应从____(填“a”或“b”)端通入。
(4)实验室用“加热氯化铵和熟石灰的固体混合物”的方法制取氨气,则其发生装置应选择_____(填字母),该反应的化学方程式为______。
【答案】长颈漏斗 该反应放热会加快反应速率,B装置能控制反应速率 气泡连续不断均匀放出 CaCO3+2HCl=CaCl2+H2O+CO2↑ 浓硫酸 a A 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
【解析】
(1)C装置中,甲仪器的名称是长颈漏斗,故填:长颈漏斗;
(2)实验室用双氧水和二氧化锰粉末制取氧气,该反应放热会加快反应速率,B装置能控制反应速率,发生装置常选用B而不选用C;若用E装置收集氧气,当气泡连续不断均匀放出时,才开始收集。
故填:该反应放热会加快反应速率,B装置能控制反应速率;气泡连续不断均匀放出;
(3)C装置中碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;浓硫酸具有吸水性,可用于干燥酸性或中性气体;干燥气体时应该长进短出,气体应从a端通入。
故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;浓硫酸;a;
(4)实验室用“加热氯化铵和熟石灰的固体混合物”的方法制取氨气,属于固固加热型,则其发生装置应选择A,该反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
故填:A;2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。

 名校课堂系列答案
名校课堂系列答案【题目】某兴趣小组想证明稀硫酸与氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应,请你参与他们的探究活动。
(设计实验)

(1)探究稀硫酸与氢氧化钠溶液的反应:
当观察到图一烧杯中出现_____的现象时,可确定稀硫酸与氢氧化钠溶液发生了化学变化,反应的化学方程式为:_____。
(2)探究实验后烧杯内是否存在过量的硫酸:
同学们设计以下实验方案:
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 稀硫酸过量 |
上述设计的实验方案中,正确的是_____(填“方案一”或“方案二”),另外一个实验方案错误的原因是_____。
(交流与反思)图二是小明和老师一起向氢氧化钠溶液中逐渐滴入稀硫酸时用数字化实验测定的反应溶液温度(T)和pH的变化曲线。
(1)在0﹣60秒pH变化不大可能的原因是_____。
(2)从图二你还能获得的一条信息是_____。