题目内容
【题目】工业上通常用高温加热碳酸钙制取生石灰。甲取碳酸钙200g高温加热一段时间后测得剩余固体质量为156g,乙将剩余固体继续高温加热至完全反应。请你回答下列问题:
(1)写出制取生石灰的化学方程式______________________________________________;
(2)甲实验时产生的气体质量为_________________g;
(3)根据甲产生的气体质量列出解参加反应的碳酸钙的质量(x)的比例式__________;
(4)乙加热完全反应后得到固体的质量为__________;
(5)甲、乙两同学实验时消耗碳酸钙的质量比为__________。
【答案】 CaCO3![]() CaO+CO2↑ 44g 100/44=x/44g 112g 1:1
CaO+CO2↑ 44g 100/44=x/44g 112g 1:1
【解析】【解答】(1)工业上通常用高温加热碳酸钙制取生石灰,反应的化学方程式是:CaCO3![]() CaO+CO2↑;(2)由质量守恒定律可知生成的二氧化碳的质量为:200g-156g=44g;
CaO+CO2↑;(2)由质量守恒定律可知生成的二氧化碳的质量为:200g-156g=44g;
(3)设参加反应的碳酸钙的质量为x,生成的氧化钙的质量为y,
CaCO3![]() CaO+CO2↑
CaO+CO2↑
100 56 44
x y 44g
参加反应的碳酸钙的质量(x)的比例式是: ![]() , x=100g;
, x=100g;
![]() ,y=56g;
,y=56g;
(4)乙同学分解的碳酸钙的质量为200g-100g=100g;
设乙同学分解碳酸钙生成的氧化钙的质量为z,
CaCO3![]() CaO+CO2↑
CaO+CO2↑
100 56
100g z
![]() , z=56g;
, z=56g;
乙加热完全反应后得到固体的质量为:56g+56g=112g;
(5)甲、乙两同学实验时消耗碳酸钙的质量比为100g:100g=1:1

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】如图是测定空气中氧气含量的两套实验装置,请据图回答下列问题(提示:铜粉在加热条件下会与氧气反应生成黑色氧化铜固体):
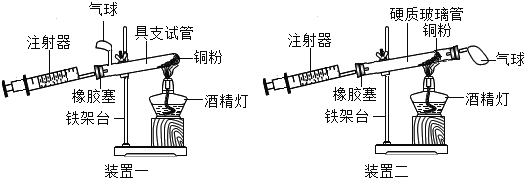
(1)装置一和装置二中气球的位置不同,_____(填“装置一”或“装置二”)更合理,理由是_____.
(2)根据实验测得的相关数据(见下表),计算空气中氧气的体积分数.
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
25mL | 15mL | 7mL | _____ |