��Ŀ����
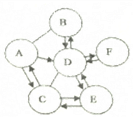
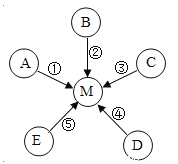
����Ŀ����ͼ�еĢ����ڷֱ�����Ԫ�ء���Ԫ�������ڱ��е���Ϣ��A��B��C��D���������ӽṹʾ��ͼ������ش��������⣺
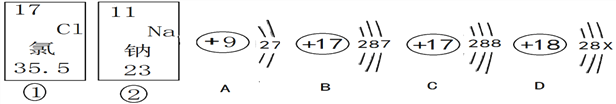
(1)��Ԫ�ص�ԭ������Ϊ__________����������ԭ�ӽṹʾ��ͼ_________________����ԭ�ӵ�������Ϊ__________����Ԫ�ص�ԭ���ڻ�ѧ�仯������___________(�����õ�������ʧȥ��)�����γ����ӣ����ӷ���Ϊ____________��
(2)ʾ��ͼD�е���=____________��
(3)A��B��C��D������ͬ��Ԫ�ص�������________��________(�����)����������ȶ��ṹ����____________��_________(�����)��
(4)A��B�������ӵ�����������______________���������Ǿ������ƵĻ�ѧ���ʡ�
���𰸡� 11 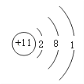 12 ʧȥ Na+ 8 B C C �������10��D ���(��Ϊ7)
12 ʧȥ Na+ 8 B C C �������10��D ���(��Ϊ7)
��������(1) ��Ԫ�����ڱ��У�Ԫ�����Ƶ����Ͻǵ�����ΪԪ�ص�ԭ�����������Ͻ�ΪԪ�ط��ţ��±���Ԫ�ص����ԭ��������ͬһԭ���У�������=���������=�˵����=ԭ��������������Ԫ�ص�ԭ������Ϊ11��ԭ�ӽṹʾ��ͼ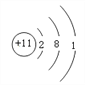 �����ԭ������=������+����������ԭ�ӵ�������Ϊ23-11=12��ԭ�ӵĻ�ѧ������Ҫ������������������������������С��4ʱ����Ӧ����ʧȥ���ӳ�Ϊ�����ӣ���Ԫ�ص�ԭ���ڻ�ѧ�仯������ʧȥ�����γ����ӣ����ӷ���ΪNa+��(2)ʾ��ͼD�еĦ�=8��(3) ����������ԭ�ӵ����A��B��C��D������ͬ��Ԫ�ص�������B��C��ԭ�Ӻ���ֻ��һ�����Ӳ��ҵ�����Ϊ2����������������Ϊ8�ĽṹΪ�ȶ��ṹ���ʾ�������ȶ��ṹ����C��D��(4)A��B�������ӵ�������������ȣ��������Ǿ������ƵĻ�ѧ���ʡ�
�����ԭ������=������+����������ԭ�ӵ�������Ϊ23-11=12��ԭ�ӵĻ�ѧ������Ҫ������������������������������С��4ʱ����Ӧ����ʧȥ���ӳ�Ϊ�����ӣ���Ԫ�ص�ԭ���ڻ�ѧ�仯������ʧȥ�����γ����ӣ����ӷ���ΪNa+��(2)ʾ��ͼD�еĦ�=8��(3) ����������ԭ�ӵ����A��B��C��D������ͬ��Ԫ�ص�������B��C��ԭ�Ӻ���ֻ��һ�����Ӳ��ҵ�����Ϊ2����������������Ϊ8�ĽṹΪ�ȶ��ṹ���ʾ�������ȶ��ṹ����C��D��(4)A��B�������ӵ�������������ȣ��������Ǿ������ƵĻ�ѧ���ʡ�

����Ŀ������˵����ȫ��ȷ����
A�������Ļ�ѧʽ��Ne2 2����ԭ�ө���2Ne | B������Ԫ�صĻ�ѧ���ʩ���ԭ�ӵĺ�������� ����Ԫ�����ڱ�Ԫ������˳������������ |
C��ˮ�������⡢��Ԫ����� �Ȼ��Ʃ������Ȼ������ӹ��� | D�����ө����������ʻ�ѧ���ʵ���С���� ԭ�ө�����ѧ�仯�еĵ���С���� |
A. A B. B C. C D. D