题目内容
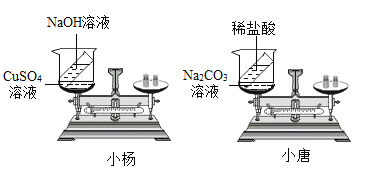
【题目】某补钙剂的主要成分是碳酸钙。欲测定该补钙剂中碳酸钙的质量分数,某同学进行了如图所示的操作(假设其它成分可溶于水但不参与反应)。
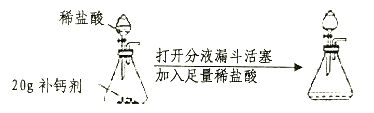
反应前的总质量:370g 反应后的总质量:363.4g
(1)该实验中,装置的气密性对测定结果______(填“有”或“无”)影响。
(2)计算该补钙剂中碳酸钙的质量分数______。
【答案】无影响 75%
【解析】
解:(1)该实验操作是通过反应前后装置的差量(即二氧化碳的质量)来计算补钙剂中碳酸钙的质量分数,要求生成的二氧化碳逸出,所以装置的气密性对测定结果无影响。
(2)根据质量守恒定律,生成二氧化碳的质量是:370g-363.4g=6.6g,设该补钙剂中碳酸钙的质量为x,
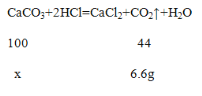
![]() =
=![]() ,解得x= 15g
,解得x= 15g
该补钙剂中碳酸钙的质量分数为:![]() ×100%=75%
×100%=75%
答:(1)该实验中,装置的气密性对测定结果无影响。
(2)该补钙剂中碳酸钙的质量分数是75%。

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案【题目】小红在探究碱的化学性质时,将稀盐酸滴入到氢氧化钠溶液中,意外地发现有气泡产生,她认为氢氧化钠溶液已经变质。氢氧化钠溶液变质的原因是______(用化学方程式表示)。
小红对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一:氢氧化钠部分变质,变质后的溶液中含有![]() 和
和![]()
猜想二:氢氧化钠全部变质,变质后的溶液中只含有![]()
(实验设计)为了验证猜想一,小红设计了如下方案:取少量变质后的氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色变红色,说明溶液中含有氢氧化钠,氢氧化钠部分变质。小敏认为小红的实验方案不合理,理由是______。
(实验与结论)小敏另外设计实验方案验证猜想二,请你帮她完成下面的实验报告:
实验步骤 | 实验现象 | 结论 |
实验1:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的氧化钙溶液并振荡 | 有白色沉淀产生 | 猜想二正确 |
实验2:将实验1试管中的混合物过滤,______ | _______ |
实验1反应的化学方程式是______。