题目内容
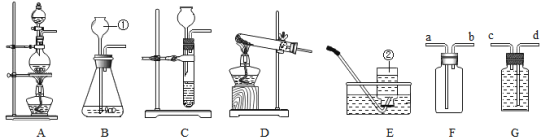
【题目】下图是与铁的性质有关的部分实验。请回答。
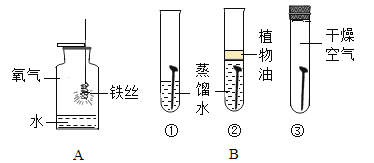
(1)A中铁丝燃烧的化学方程式为___________,集气瓶中预先放少量水的目的是_______。
(2)B是探究铁钉锈蚀条件的实验。通过对比①③试管中的现象,可知铁钉生锈需要与_____________接触。写出一种日常生活中防止铁制品锈蚀的方法_______________。
(3)已知锰(Mn)的金属活动性介于镁和锌之间,如果通过实验验证铁和锰的金属活动性强弱,能达到实验目的的试剂组是_______________(填字母)。
A.Mn Fe SO4溶液 B.Mn Fe MgSO4溶液 C.Mn Fe ZnSO4溶液
(4)在我国,用金属制造硬币己有几千年的历史。为了延长硬币的使用寿命,请分别从物理性质、化学性质的角度分析,用于铸造硬币的金属材料应具有的性质。

①从物理性质的角度分析,应具有的性质是_____________________。
②从化学性质的角度分析,应具有的性质是_____________________。
【答案】3Fe+2O2![]() Fe3O4 防止生成的高温融化物溅落炸裂瓶底. 水 喷漆(合理即可给分) AC 硬度大(多答其他不扣分) 化学性质稳定,不易与空气中的氧气等物质反应(答出一点即可得分)
Fe3O4 防止生成的高温融化物溅落炸裂瓶底. 水 喷漆(合理即可给分) AC 硬度大(多答其他不扣分) 化学性质稳定,不易与空气中的氧气等物质反应(答出一点即可得分)
【解析】
(1)A中铁丝燃烧生成四氧化三铁,化学方程式为3Fe+ 2O2 ![]() Fe3O4,铁在氧气中燃烧放出大量热,火星四射,集气瓶中预先放少量水的目的是防止生成的高温融化物溅落炸裂瓶底;
Fe3O4,铁在氧气中燃烧放出大量热,火星四射,集气瓶中预先放少量水的目的是防止生成的高温融化物溅落炸裂瓶底;
(2)B是探究铁钉锈蚀条件的实验。①中铁、氧气、水充分接触,铁生锈,③中没有水,铁不生锈,对比①③试管中的现象,可知铁钉生锈需要与水接触。日常生活中防止铁制品锈蚀的方法有隔绝氧气(如刷漆)、保持金属表面洁净干燥、改变金属的组成和结构(制成合金);
(3)A.Mn 和FeSO4溶液不反应,证明铁活动性比锰的弱;
B.Mn 和Fe 都不与MgSO4溶液反应,只能证明锰和铁的活动性都比镁的弱,但不能证明铁和锰的活动性强弱;
C.Mn 和ZnSO4溶液反应,证明锰的活动性比锌的强,Fe和ZnSO4溶液不反应,证明铁的活动性比锌的弱,因此可以证明锰的活动性比铁的强,选AC;
(4)①从物理性质的角度分析,熔点比较低,容易铸造,光泽好,硬度比较大,不易磨损;
②从化学性质的角度分析,应具有的性质是在通常情况下化学性质比较稳定,不容易生锈。

 优加精卷系列答案
优加精卷系列答案【题目】物质丙是重要的化工产品,在国民经济中占有重要地位。工业上用甲和乙合成内。甲、乙、内的微观示意图见下表。
物质 | 甲 | 乙 | 丙 |
|
微观示意图 |
|
|
|
(l)甲、乙、丙中属于化合物的是(填序号)______。
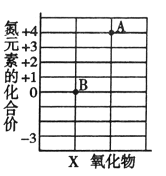
(2)已知物质丙中氢元素的化合价为![]() 。则另一种元素的化合价为______。
。则另一种元素的化合价为______。
(3)现有![]() 的甲和
的甲和![]() 的乙混合反应制取内,反应一段时间后,经测定剩余甲的质量为
的乙混合反应制取内,反应一段时间后,经测定剩余甲的质量为![]() ,则剩余乙的质量为______g。
,则剩余乙的质量为______g。