题目内容
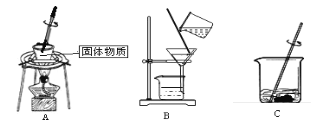
【题目】实验室里既可用高锰酸钾(或氯酸钾和二氧化锰的混合物)在加热条件下使其分解制取氧气,也可用如图装置,通过分解过氧化氢(H2O2)来制取氧气。
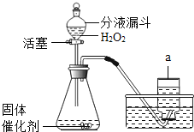
请你根据已学化学知识和经验回答下列问题:
(1)写出过氧化氢分解的化学方程式: 。
(2)写出如图装置中仪器a的名称: 。
(3)与高锰酸钾(或氯酸钾和二氧化锰的混合物)制取氧气相比,用过氧化氢制取氧气的优点是: 。
(4)收集氧气的方法还可用 法,你选择此方法的理由是: 。
(5)如图发生装置还可以用于制取的气体有 。
【答案】(l)2H2O22H2O+O2↑ (写MnO2为催化剂亦可);
(2)集气瓶;
(3)不加热(或节约能源、操作简单)不产生污染物(或绿色环保)(其它合理答案亦可)
(4)向上排空气,氧气密度比空气大;
(5)二氧化碳(CO2)(其它合理答案亦可)
【解析】
试题分析:(1)过氧化氢制氧气的反应物是过氧化氢,生成物是水和氧气,反应条件是二氧化锰作催化剂,用观察法配平,氧气后面标上上升符号;
(2)要熟记常见仪器的名称,用来收集气体的是集气瓶;
(3)高锰酸钾制氧气需要加热,操作复杂,不安全,而过氧化氢制氧气不需加热,操作简单,安全;
(4)收集方法的选择是根据:难溶于水或不易溶于水用排水法收集,密度比空气大用向上排空气法收集,密度比空气小用向下排空气法收集,由于氧气密度比空气大,用向上排空气法收集;
(5)反应物的状态是固体和液体,不需要加热,如果固体与固体反应制取气体需要加热,由于制取二氧化碳是盐酸和大理石,也不需要加热,故可制取二氧化碳。

练习册系列答案
相关题目