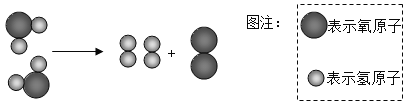题目内容
【题目】能源“非石油化”是战略目标,发展以CH4、CO2等原料的 “C1化学”成为当今化工生产的必然趋势。通常天然气中含有H2S等有毒气体,下图为天然气合成氨(NH3)的工艺流程:
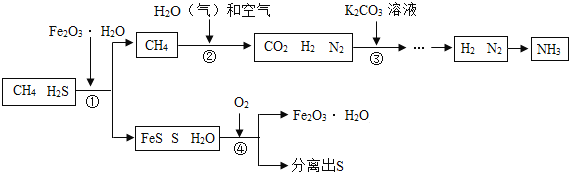
(1)合成氨的原料之一为氮气,该流程中为合成氨提供氮气的物质是 。
(2)①处加入Fe2O3·H2O的目的是 。
(3)②处CH4与H2O(气)反应生成CO2、H2,反应的化学方程式是(反应条件略去) 。
(4)③处一般加入K2CO3溶液以吸收CO2 ,K2CO3溶液与CO2反应生成碳酸氢钾(KHCO3),该反应的化学方程式是 。
(5)该流程中参与循环的物质是 。
【答案】(1)空气 (2)除去硫化氢(H2S) (3)CH4+2H2O = CO2+4H2
(4)K2CO3+CO2+ H2O =2KHCO3 (5)Fe2O3·H2O
【解析】
试题分析:(1)根据图示分析,在②处加入了空气,再结合空气的成分分析,空气中有大量的氮气,所以该流程中为合成氨提供氮气的物质是空气;
(2)根据图示分析,天然气中含有的H2S气体是有毒的气体,不能排放到大气中,故通过加入Fe2O3H2O可反应生成硫化亚铁,而除去H2S;
(3)根据题意②处CH4与H2O(气)反应生成CO2和H2,故反应的化学方程式为CH4+2H2O= CO2+4H2。
(4)根据题意K2CO3溶液与CO2反应生成碳酸氢钾(KHCO3),结合质量守恒定律中的元素守恒可知,反应中应该有水的参加,故反应的化学方程式为K2CO3+CO2+ H2O=2KHCO3。
(5)根据图示分析,在该流程中加入了Fe2O3H2O,最后又生成了Fe2O3H2O,所以,该流程中参与循环的物质是Fe2O3H2O。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案【题目】小明同学查阅了![]() 和
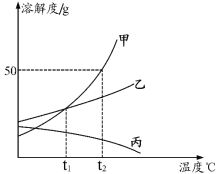
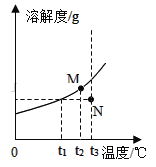
和![]() 在不同温度时的溶解度,并绘制出相应的溶解度曲线。
在不同温度时的溶解度,并绘制出相应的溶解度曲线。
温度/℃ | 20 | 30 | 50 | 60 | 80 | |
溶解度/g |
| 34 | 37 | 42.6 | 45.5 | 51.1 |
| 31.6 | 45.8 | 85.5 | 110 | 169 | |
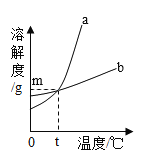
回答下列问题:
(1)图中表示![]() 溶解度曲线的是_____(填a或b)
溶解度曲线的是_____(填a或b)
(2)60℃时,将![]() 和
和![]() 的饱和溶液同时降温到20℃,则所得溶液中溶质的质量分数大小关系是
的饱和溶液同时降温到20℃,则所得溶液中溶质的质量分数大小关系是![]() _____
_____![]() (填“大于”、“等于“或“小于”)
(填“大于”、“等于“或“小于”)
(3)![]() 和
和![]() 在t
在t
(4)30℃时,将![]() ,固体放入100g水中充分溶解,所得溶液中溶质的质量分数为_____(计算结果精确到0.1%)
,固体放入100g水中充分溶解,所得溶液中溶质的质量分数为_____(计算结果精确到0.1%)