题目内容
【题目】将CO和CO2的混合气体10g,在高温下缓慢通过足量的氧化铁后,再把得到的气体通入足量的澄清石灰水中,过滤、干燥,得到30g白色沉淀,则原混合气体中CO 和 CO2的质量比为
A.14∶11B.7∶11C.2∶1D.1∶2
【答案】A
【解析】
过滤,干燥,得到30g白色沉淀是碳酸钙,
设通入足量的澄清石灰水中的二氧化碳的质量为X,
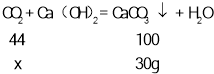
![]() 解得X=13.2g,
解得X=13.2g,
通过计算可知,CO和CO2的混合气体10g在高温下缓慢通过足量的氧化铁后,气体质量增加了:13.2g-10g=3.2g,
由CO→CO2可知,
当有28份质量的一氧化碳转化成二氧化碳后,增加的质量为:44份-28份=16份,
设一氧化碳的质量为y,根据题意有:

![]()
y=5.6g,
所以,原混合气体中,一氧化碳的质量是5.6g,二氧化碳的质量是10g-5.6g=4.4g;
则原混合气体中CO和CO2的质量比为:5.6g:4.4g=14:11。
故选:A。

 走进文言文系列答案
走进文言文系列答案【题目】工业上以高纯度的二氧化锰为原料制备高锰酸钾的主要流程如下:

已知相关物质的溶解度(20℃)如下表:
物质 | K2CO3 | K2SO4 | KMnO4 |
溶解度/g | 111 | 11.1 | 6.34 |
(1)KMnO4中锰元素的化合价为_____.
(2)操作I的名称是_____.“干燥”过程中温度不宜过高的原因是_____(用化学方程式表示).
(3)“通CO2酸化”,反应的化学方程式为:3K2 MnO4+2CO2═2KMnO4+MnO2↓+2K2CO3;不用稀H2SO4酸化,反应的化学方程式为:3K2 MNO4+2H2SO4═2KMnO4+MnO2↓+2K2SO4+2H2O;工业上不采用稀H2SO4酸化的原因是_____.
(4)电解法也可以实现由K2MnO4向KMnO4的转化,反应的化学方程式为:2K2 MnO4+2H2O![]() 2KMnO4+2KOH+H2↑,与“通CO2酸化”相比,其优点是_____.
2KMnO4+2KOH+H2↑,与“通CO2酸化”相比,其优点是_____.
【题目】水是宝贵的自然资源,我们要认识它,爱护它。
(1)水是由______组成的,电解水的化学方程式是________
(2)硬水不利于我们的生活,生活中我们可以用____的方法将其软化
(3)请推荐你在生活中节约用水的一个好举措______
(4)自然界的水因含有多种杂质而不能直接饮用。需要经过自来水厂处理后才能饮用。目前很多自来水厂用氯气进行消毒。消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:

若D的化学式为HClO,写出图甲所示反应的化学方程式 。小军将新制的氯气通入紫色石蕊试液中,惊奇地发现试液先变红,接着就褪色了。他查阅资料得知新制的氯水具有漂白性。为探究溶液褪色的原因,他设计了几个实验:
(实验准备)用紫色石蕊试液浸泡几朵小纸花,并晾干;加热少量新制的氯水,冷却后灌入喷壶。
实验Ⅰ | 实验Ⅱ | 实验Ⅲ | 实验Ⅳ | 实验Ⅴ |
|
|
|
|
|
(实验现象)①实验Ⅰ:_______________________ ②实验Ⅱ、Ⅲ:紫花不变色
③实验Ⅳ:紫花先变红后褪色 ④实验Ⅴ:紫花变红,不褪色
(实验结论)新制氯水中具有漂白性的物质是______________(写化学式)。