题目内容
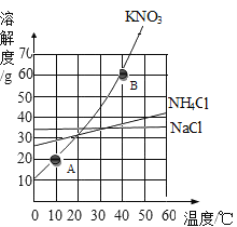
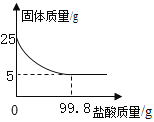
【题目】为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入125g稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:
(1)这种贝壳中碳酸钙的质量分数是_____。
(2)25g贝壳与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数是____。
【答案】 80% 20%
【解析】由图可以看固体减少了20g,即碳酸钙的质量为20g,根据碳酸钙的质量和对应的化学方程式求算氯化钙和二氧化碳的质量,进而求算对应的质量分数。由图可以看出固体减少了20g,即碳酸钙的质量为20g,所以贝壳中碳酸钙的质量分数为![]() ×100%=80%;
×100%=80%;
设恰好反应时,生成氯化钙的质量为x,同时产生二氧化碳的质量为y,CaCO3+2HCl=CaCl2+CO2↑+H2O
100 11144
20g x y
![]() ,
, ![]()
x=22.2g,y=8.8g
所得溶液中溶质的质量分数=![]() ×100%=20%
×100%=20%
答:(1)这种贝壳中碳酸钙的质量分数是 80%;
(2)25g贝壳与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数为20%。

【题目】为了探究相同条件下同种溶质在不同溶剂中的溶解性,某兴趣小组同学进行如下两组实验。(提示:本实验所川汽油与KMnO4、碘均不发生化学反应)
【实验l】KMnO4晶体在不同溶剂中的溶解实验
根据实验步骤、实验操作图示填写相关实验现象。
实验步骤 | 实验操作图示 | 实验操作及现象 |
步骤1 |
| 振荡后静置: |
步骤2 |
| 将步骤1中A试管内溶液倒人B试管中,振荡后静置:(2)B试管中观察到的现象为__________。 |
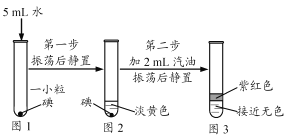
【实验2]碘在不同溶剂中的溶解实验
根据实验操作图示回答相关问题。
实验操作图示 | 实验结论或解释 |
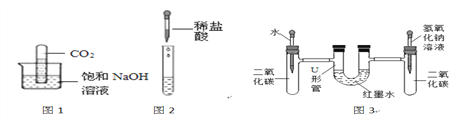
| (3)由图2所示现象叮知:碘_____(选填“不”、“微”或“易”)溶于水 |
【反思与应用】
(5)①碘易溶于酒精。若【实验2】中汽油用酒精代替,振荡后静置,最终所得液体______(选填“分层”或“小分层”)。
②“从稀碘水巾提取碘”是“海带提碘”工艺巾的一个重要步骤,其原理类似【实验2]中第二步操作。工业实际生产时使用其他挥发性液体代替汽油,这种挥发性液体必须具备的条件是________。