题目内容
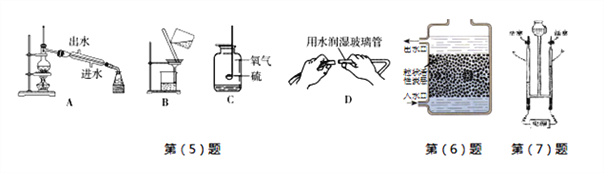
【题目】根据下列装置图,回答有关问题:
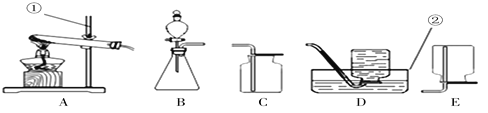
(1)请写出仪器的名称:①_________,②_______。
(2)若选用B装置作为制取氧气的发生装置,其化学方程式是_______________。
(3)用高锰酸钾制取氧气:化学方程式为_________________;如果用A作为发生装置则需________________;如果用D装置收集氧气,当气泡连续均匀冒出时才能收集的原因是______________。
【答案】 铁架台 水槽 略 略 在试管口放一团棉花 开始时冒出的气泡主要是空气(或防止收集到的氧气不纯)
【解析】(1)根据常见仪器的名称和作用进行分析;(2)根据B装置为固液常温型装置,故实验室用过氧化氢在二氧化锰的催化作用下生成水和氧气,写出反应的化学方程式即可;(3)根据高锰酸钾加热生成锰酸钾、二氧化锰和氧气写出化学方程式以及用高锰酸钾制取氧气时的注意事项进行分析。
(1)图中仪器的名称:①是铁架台;②是水槽;(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,因为反应物是固体和液体,不需要加热,所以发生装置选B,反应的化学方程式为: ![]()
![]()
![]() , (3)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的方程式是:
, (3)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的方程式是: ![]()
![]()
![]() ,如果用A作为发生装置则需在试管口放一团棉花,以防高锰酸钾粉末进入导管;利用排水法收集气体时,刚出现气泡时不能立即收集,因为这时排出的气体主要是空气,当气泡连续均匀冒出时方可开始收集。
,如果用A作为发生装置则需在试管口放一团棉花,以防高锰酸钾粉末进入导管;利用排水法收集气体时,刚出现气泡时不能立即收集,因为这时排出的气体主要是空气,当气泡连续均匀冒出时方可开始收集。

【题目】某小组对H2O2溶液制取氧气进行了如下探究:
【探究一】:探究不同催化剂对H2O2分解快慢的影响
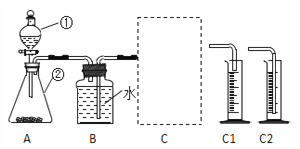
该小组采用了如下图所示装置进行实验,实验中催化剂均为0.4g,H2O2溶液浓度均为10%20mL,在C框中连接导管和量筒,并测量收集到50mL水时的某项数据,经计算后的数据如下表:
催化剂种类 | 气体产生速率(mL/s) |
二氧化锰 | 3.5 |
氧化铜 | 4.5 |
活性炭 | 5.8 |
(1)检查A装置气密性的方法是:用弹簧夹夹住A装置右侧导气管,打开①的两个活塞,向其中加水,若___________,则气密性良好。
(2)C框内选用C1或C2装置,对该探究实验结论有无影响______。
(3)从实验数据可知:相同条件下表中催化剂的催化效果由强到弱依次为________。
(4)该探究实验中,需要测定的数据是____________。
(5)当量筒中收集到50mL水时,双氧水分解出的氧气体积______50mL(填“大于”、“等于”、“小于”)。
【探究二】:探究H2O2溶液浓度对分解速率的影响
如图:在250mL三颈瓶中,加入MnO2均为0.5g,在恒压漏斗中加入不同浓度的H2O2溶液各20mL分别进行实验。并用温度传感器测量并绘制出瓶内温度与时间关系图。如下图所示。
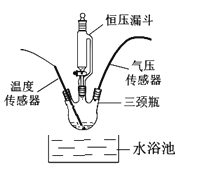
再将该装置的三颈瓶浸入水浴池中(该池可使瓶内的溶液温度恒定在20℃),用上述实验中相同量的各物质重复上述实
验,用气压传感器测量并绘制出瓶内气压与时间关系图。如下图所示。
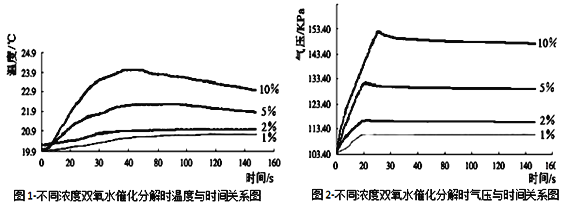
(6)实验中,恒压漏斗的作用是__________。
(7)由图1知道:H2O2溶液分解时会_________热量(填“放出”或“吸收”)。
(8)由图2知道: H2O2溶液浓度越高,其分解反应速率越______(填“快”或“慢”),以10%H2O2溶液为例,20S后三颈瓶内气压约由高缓慢降低的原因是_________。
(9)影响H2O2溶液分解速率的因素,除了催化剂的种类、H2O2溶液浓度外,还可能有的因素如:__________(请写出一种)。
【题目】化学兴趣小组在实验室用氯酸钾和二氧化锰混合加热制取氧气,该反应的化学表达式为________。某次实验时偶然发现制得的气体有刺激性气味,这一现象引起了同学们的兴趣,于是在老师的指导下对该气体成分进行探究。
【提出问题】氯酸钾与二氧化锰混合加热后产生的气体成分是什么?
【查阅资料】
①氯酸钾与二氧化锰混合加热产生的气体只以单质形式存在;
②氯气(Cl2)是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
【猜想假设】
猜想一:该气体为O2;猜想二:该气体为______;猜想三:该气体为O2和Cl2的混合物。
【实验探究】
序号 | 操作 | 现象 | 结论 |
方案Ⅰ | 用排水集气法收集甲、乙两瓶气体,将带火星的木条伸入甲瓶,湿润的淀粉碘化钾试纸伸入乙瓶。 | 木条复燃, 淀粉碘化钾试纸不变色 | 猜想_______成立 |
方案Ⅱ | 向上排空气法收集甲、乙两瓶气体,将带火星的木条伸入甲瓶,湿润的淀粉碘化钾试纸伸入乙瓶。 | 木条______, 淀粉碘化钾试纸为___色 | 猜想三成立 |
【反思评价】
为什么两种方案得出的结论不一致?哪个是正确的?
①同学:方案Ⅰ结论不正确,其操作不合理,不合理之处是__________。
②老师:不需要进行实验,就能排除猜想一,理由是__________。
【拓展应用】
实验结束后,该组同学准备回收固体剩余物中的不溶物二氧化锰,实验的主要步骤为:①溶解、②________、③洗涤干燥。步骤②中玻璃棒的作用是_________。