题目内容
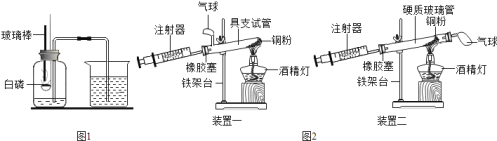
【题目】如图1是“空气中氧气体积分数测定”实验的改进装置。主要操作是:在实际容积为150mL的集气瓶里,先装进50mL的水,再按图1连好仪器,按下热的玻璃棒,白磷立即被点燃。(白磷40℃即燃烧,燃烧产物与红磷相同)
(1)白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是________,若实验成功,最终集气瓶中水的体积约为______mL。
(2)该实验可推论出氮气的物理性质为________,化学性质为________。
(3)若将白磷换成炭粉,该实验能否获得成功?为什么?_________________。
(4)集气瓶里预先装进的50mL水,在实验过程中起到哪些作用?__________(填写序号)
A.加快集气瓶内气体冷却B.液封导气管末端以防气体逸出C.吸收五氧化二磷
(5)图2是另一实验小组对测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题。(已知铜和氧气在加热的条件下反应生成氧化铜固体)
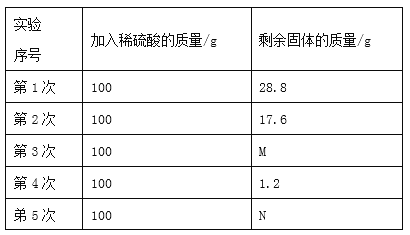
①根据下表提供的实验数据,完成如表:
硬质玻璃管中 空气的体积 | 反应前注射器中 空气体积 | 反应后注射器中 气体体积 | 实验测得空气中 氧气的体积分数 |
25mL | 15mL | 9mL |
②装置一和装置二中气球的位置不同,_________(填“装置一”或“装置二”)更合理,理由是_______。
【答案】先下降,后上升; 70。 氮气难溶于水; 化学性质不活泼。 不能;因为碳燃烧产生气体,使瓶中大气压不变。 ABC 装置二; 能让空气更易流通,全部通过铜粉,使氧气与铜粉充分反应
【解析】
(1)白磷燃烧放出热量,集气瓶内温度升高,压强变大,一部分水进入导气管中,导致集气瓶内液面下降。白磷燃烧消耗氧气,无气体生成,冷却至室温后,集气瓶内压强变小,打开止水夹,烧杯中的水进入集气瓶中,所以集气瓶内的液面上升。集气瓶内空气的体积是150mL-50ml=100ml,其中氧气的体积是100ml×![]() =20ml,则进入水的体积是20ml,所以最终集气瓶中水的体积约为50ml+20mL=70ml(2)该实验可推论出氮气难溶于水,化学性质不活泼。(3)测定空气中氧气含量所选物质应该是只与氧气反应,且无气体生成,如果用炭粉代替白磷,因为碳燃烧产生气体,使瓶中大气压不变,水不会进入集气瓶中,无法测定空气中氧气的体积含量。(4)集气瓶里预先装进的50mL水,可加快集气瓶内气体冷却、液封导气管末端以防气体逸出、吸收五氧化二磷,故选ABC。(5)①注射器内气体减少的体积就是氧气的体积,则实验测得空气中氧气的体积分数为:
=20ml,则进入水的体积是20ml,所以最终集气瓶中水的体积约为50ml+20mL=70ml(2)该实验可推论出氮气难溶于水,化学性质不活泼。(3)测定空气中氧气含量所选物质应该是只与氧气反应,且无气体生成,如果用炭粉代替白磷,因为碳燃烧产生气体,使瓶中大气压不变,水不会进入集气瓶中,无法测定空气中氧气的体积含量。(4)集气瓶里预先装进的50mL水,可加快集气瓶内气体冷却、液封导气管末端以防气体逸出、吸收五氧化二磷,故选ABC。(5)①注射器内气体减少的体积就是氧气的体积,则实验测得空气中氧气的体积分数为:![]() ×100%=15%。②装置二与装置一比较,装置二中的气球在玻璃管的后部,更易让空气流通,使氧气与铜能充分反应。
×100%=15%。②装置二与装置一比较,装置二中的气球在玻璃管的后部,更易让空气流通,使氧气与铜能充分反应。