题目内容
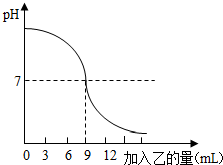 已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示:向盛有10mL稀的甲溶液(其中滴有少量紫色石蕊试剂)中,加入乙溶液时,溶液pH的变化曲线,请分析曲线回答问题:
已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示:向盛有10mL稀的甲溶液(其中滴有少量紫色石蕊试剂)中,加入乙溶液时,溶液pH的变化曲线,请分析曲线回答问题:(1)甲是
(2)当加入乙溶液的体积为
(3)当溶液的pH=1.4时,溶液中的溶质是(指示剂除外)
考点:中和反应及其应用,溶液的酸碱性与pH值的关系,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:(1)氢氧化钠溶液显碱性,pH>7,;
显碱性的溶液能使石蕊试液变蓝色;
(2)氢氧化钠和稀盐酸反应生成氯化钠和水,氯化钠溶液显中性;
(3)显酸性的溶液pH<7.
显碱性的溶液能使石蕊试液变蓝色;
(2)氢氧化钠和稀盐酸反应生成氯化钠和水,氯化钠溶液显中性;
(3)显酸性的溶液pH<7.
解答:解:(1)因为甲溶液的pH>7,所以甲是氢氧化钠溶液;滴有少量紫色石蕊,试剂甲溶液呈蓝色.
故填:氢氧化钠;蓝.
(2)当加入乙溶液的体积为9mL时,甲、乙溶液恰好完全反应,溶液的pH=7,氢氧化钠和稀盐酸反应的化学方程式为:NaOH+HCl═NaCl+H2O.
故填:9;NaOH+HCl═NaCl+H2O.
(3)当溶液的pH=1.4时,说明稀盐酸过量,溶液中的溶质是氯化钠和氯化氢.
故填:氯化钠和氯化氢.
故填:氢氧化钠;蓝.
(2)当加入乙溶液的体积为9mL时,甲、乙溶液恰好完全反应,溶液的pH=7,氢氧化钠和稀盐酸反应的化学方程式为:NaOH+HCl═NaCl+H2O.
故填:9;NaOH+HCl═NaCl+H2O.
(3)当溶液的pH=1.4时,说明稀盐酸过量,溶液中的溶质是氯化钠和氯化氢.
故填:氯化钠和氯化氢.
点评:实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
一包白色粉末,可能含有CaCO3,BaCl2,Na2SO4,Na2CO3,K2SO4等物质,某同学对其进行了探究实验,实验过程如图:
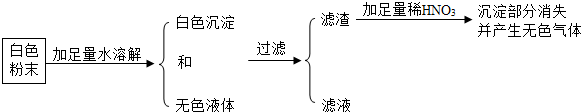
则该同学推测此白色粉末,至少由 种物质组成,其中一定含有的物质是 .

则该同学推测此白色粉末,至少由
环境问题是全球共同关注的问题,环境污染的发生、危害与防治都与化学有关.根据有关的化学知识,下列措施和理由之间,因果关系不正确的是( )
| A、严禁排放未经处理的有毒工业废水--防止水土流失 |
| B、不允许焚烧农作物秸杆--防止污染空气 |
| C、限制生产含磷洗涤剂--防止湖海出现“赤潮” |
| D、限制排放不符合尾气排放标准的气体--防止污染空气 |
小红查阅资料获得信息:(1)2Na+Cl2
2NaCl(2)2Mg+CO2
2MgO+C.通过这两个反应形成四点认识,其中正确的是( )
①工业上常用反应(1)生产食盐
②反应(2)属于置换反应
③燃烧不一定要有氧气参与
④不是所有燃烧都可用CO2灭火.
| ||
| ||
①工业上常用反应(1)生产食盐
②反应(2)属于置换反应
③燃烧不一定要有氧气参与
④不是所有燃烧都可用CO2灭火.
| A、只有①②④ | B、只有②④ |
| C、只有②③④ | D、只有①③ |
下列做法没有科学依据的是( )
| A、烧柴火时为了节约燃料将柴火堆得严严实实 |
| B、进入久未开启的地窖前做灯火试验 |
| C、为了使石灰浆抹的墙壁快点干燥,常在室内生一个炭火盆 |
| D、将木桩埋入地下的部分表面用火烧焦 |