题目内容
一包白色粉末,可能含有CaCO3,BaCl2,Na2SO4,Na2CO3,K2SO4等物质,某同学对其进行了探究实验,实验过程如图:
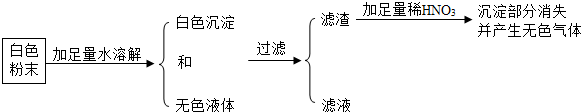
则该同学推测此白色粉末,至少由 种物质组成,其中一定含有的物质是 .

则该同学推测此白色粉末,至少由
考点:物质的鉴别、推断,盐的化学性质
专题:混合物组成的推断题
分析:根据碳酸钙为白色固体,难溶于水,氯化钡和硫酸钾、硫酸钠可以反应生成不溶于水且不溶于酸的白色沉淀;碳酸钠可以和氯化钡反应生成不溶于水但是可以溶于酸的白色固体,在书写可能的组合时,尽可能的根据题意把每一组合写出,要仔细分析每一实验步骤的用意及实验中所发生的化学反应,从而做出正确的判断.
解答:解:碳酸钙为白色固体,难溶于水,氯化钡和硫酸钾及硫酸钠可以反应生成不溶于水且不溶于酸的白色沉淀;碳酸钠可以和氯化钡反应生成不溶于水但是可以溶于酸的白色固体.
把白色粉末溶解后得无色溶液和白色沉淀,白色固体可能是碳酸钙,可能是硫酸钠、硫酸钾与氯化钡反应后生成的硫酸钡沉淀,也可能是碳酸钠和氯化钡反应生成的碳酸钡,其中碳酸钙和碳酸钡能够溶于酸,而硫酸钡不溶于酸,而题目中的白色沉淀部分溶于稀硝酸中,说明这种白色沉淀肯定含有硫酸钡,碳酸钙或碳酸钡中的一种,也可能是这两者的混合物,从而可以判断一定含有氯化钡,硫酸钾和硫酸钠至少含有一种,而碳酸钡和碳酸钠至少含有一种,所以白色粉末,至少由3种物质组成,其中一定含有的物质是:BaCl2.
故答案为:3; BaCl2.
把白色粉末溶解后得无色溶液和白色沉淀,白色固体可能是碳酸钙,可能是硫酸钠、硫酸钾与氯化钡反应后生成的硫酸钡沉淀,也可能是碳酸钠和氯化钡反应生成的碳酸钡,其中碳酸钙和碳酸钡能够溶于酸,而硫酸钡不溶于酸,而题目中的白色沉淀部分溶于稀硝酸中,说明这种白色沉淀肯定含有硫酸钡,碳酸钙或碳酸钡中的一种,也可能是这两者的混合物,从而可以判断一定含有氯化钡,硫酸钾和硫酸钠至少含有一种,而碳酸钡和碳酸钠至少含有一种,所以白色粉末,至少由3种物质组成,其中一定含有的物质是:BaCl2.
故答案为:3; BaCl2.
点评:本题为推断题,对于推断题的解法,要根据题给条件和物质的化学特性找准突破口,然后顺藤摸瓜尽可能的把没有组合写出,然后进行解答.

练习册系列答案
相关题目
液化气石油气瓶要统一加贴新标识,新标识上要含有以下选项中的( )
A、 |
B、 |
C、 |
D、 |
往AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,下列结论正确的是( )
| A、滤渣中一定有Fe粉 |
| B、滤渣中一定有Cu粉 |
| C、滤液中一定有Fe2+ |
| D、滤液中一定有Ag+、Cu2+ |
NaHSO4在水溶液中能够电离出Na+、H+和SO42-.下列对于NaHSO4的分类中不正确的是( )
| A、NaHSO4是盐 |
| B、NaHSO4是酸式盐 |
| C、NaHSO4是钠盐 |
| D、NaHSO4是酸 |
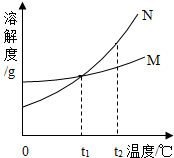 如图所示,M、N分别表示两种固体物质(不含结晶水)的溶解度曲线,试根据图中曲线判断下列说法不正确的是( )
如图所示,M、N分别表示两种固体物质(不含结晶水)的溶解度曲线,试根据图中曲线判断下列说法不正确的是( )| A、N的溶解度受温度的影响比M大 |
| B、t2℃时,M、N具有相同的溶解度 |
| C、M、N两种饱和溶液,当温度从t1降至t2后,剩余溶液的溶质质量分数相等 |
| D、M、N两种饱和溶液,当温度从t1降至t2时,一定析出相同质量的晶体 |
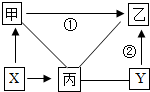 由C、H、O、Cu四种元素组成的初中常见物质,各物质之间有如图所示的关系,其中甲、乙、丙是单质,乙为紫红色固体,X、Y是氧化物.图中“-”表示相连的物质之间可发生反应,“→”表示由某一物质可制得另一物质.(反应条件已略去)请回答:
由C、H、O、Cu四种元素组成的初中常见物质,各物质之间有如图所示的关系,其中甲、乙、丙是单质,乙为紫红色固体,X、Y是氧化物.图中“-”表示相连的物质之间可发生反应,“→”表示由某一物质可制得另一物质.(反应条件已略去)请回答: 图中转化关系多涉及的都是初中化学常见物质(部分生成物已略去),其中A和B均为非金属单质,其它物质均为氧化物.
图中转化关系多涉及的都是初中化学常见物质(部分生成物已略去),其中A和B均为非金属单质,其它物质均为氧化物.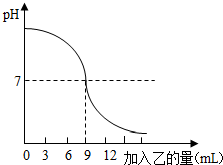 已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示:向盛有10mL稀的甲溶液(其中滴有少量紫色石蕊试剂)中,加入乙溶液时,溶液pH的变化曲线,请分析曲线回答问题:
已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示:向盛有10mL稀的甲溶液(其中滴有少量紫色石蕊试剂)中,加入乙溶液时,溶液pH的变化曲线,请分析曲线回答问题: