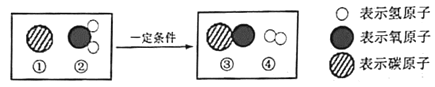
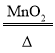题目内容
【题目】甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线如图所示。
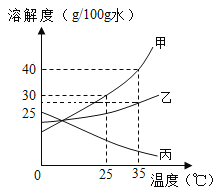
①25℃时,甲、乙、丙三种物质中溶解度最大的是__________。
②35℃时,完全溶解20g甲物质最少需要__________ g水。
③要使35℃时接近饱和的乙溶液变成该温度下的饱和溶液,可采用的方法是_______和_______。
④现有操作步骤:a.溶解;b.过滤;c.降温结晶;d.加热浓缩;若甲固体中含有少量乙,则提纯甲的操作步骤依次为__________(填字母序号)。
⑤将25℃时丙的饱和溶液升温到35℃,则其溶液的溶质质量分数__________(填“变大”、“变小”或“不变”)。
⑥35℃时,甲、乙溶液的溶质质量分数相等且均为a%,则甲溶液一定为__________(填“饱和”或“不饱和”)溶液,![]() 的取值范围为__________。
的取值范围为__________。
【答案】甲 50 增加溶质 恒温蒸发溶剂 adcb 减小 不饱和 ≤20%
【解析】
①通过分析溶解度曲线可知,25℃时,甲、乙、丙三种物质中溶解度最大的是甲;
②35℃时,甲物质的溶解度是40g,所以完全溶解20g甲物质最少需要50g水;
③乙物质的溶解度随温度的升高而增大,所以要使35℃时接近饱和的乙溶液变成该温度下的饱和溶液,可采用的方法是增加溶质和恒温蒸发溶剂;
④现有操作步骤:a.溶解 b.过滤 c.降温结晶 d.加热浓缩;甲物质的溶解度受温度变化影响较大,所以若甲固体中含有少量乙,所以提纯甲的操作步骤依次为:adcb;
⑤将25℃时丙的饱和溶液升温到35℃,丙物质的溶解度减小,有溶质析出,而溶剂质量不变,所以其溶液的溶质质量分数减小;
⑥35℃时,虽然甲肯定不是饱和溶液,但乙的最大溶质质量分数是它达到饱和状态时的数值,此时为20%,乙不饱和是小于20%,故a%≤20%。
故答案为:(1)①甲;
②50;
③增加溶质,恒温蒸发溶剂;
④adcb;
⑤减小;
⑥不饱和,≤20%

 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案【题目】研究和控制化学反应条件有重要意义。
⑴同学们想探究双氧水的浓度对反应速率的影响。在其他条件相同的情况下进行了三次实验。记录各收集一瓶相同体积氧气所需要的时间。
实验 | 30%双氧水的质量(g) | 加入水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
1 | 10 | 40 | 5 | 200 |
2 | 20 | 30 | 5 | 100 |
3 | 30 | 20 | 67 |
取用二氧化锰的仪器是

②写出上述反应的文字表达式 。
实验3中,加入二氧化锰的质量为 g。
相同条件下,实验3产生氧气的速率最快,说明 。

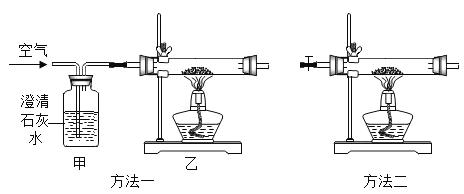
⑵同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气。为了验证加热双氧水也可以产生氧气,同学们选择上右图装置(气密性良好)进行实验。实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是 。
【题目】请设计一个实验,验证蜡烛中含有氢元素和碳元素,并填写实验报告.
(1)实验原理:________.
(2)实验用品:________.
(3)实验步骤与
假设 | 实验步骤 | 实验现象 | 分析 |
________ | ________ | ||
________ | ________ | ________ | (1)________ |
________ | ________ | ________ | (2)________ |
(4)结论:________.
(5)甲、乙、丙三瓶气体,可能是氢气、二氧化碳、氧气中的一种或几种,进行如下实验:
将带火星的木条伸入瓶内,一瓶复燃,其余二瓶没有明显现象;
将燃着的木条分别伸进瓶内,一瓶的木条燃得更旺,另二瓶气体都燃烧,在火焰上方罩一只干而冷的烧杯,烧杯内壁有水珠.
试根据上述实验的现象推断:三瓶气体中,肯定没有________,一定有________.