题目内容
【题目】下列化学方程式中书写正确的是( )。
A. P+O2![]() P2O5B. 2KMnO4
P2O5B. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
C. 2H2O=2H2+O2D. Fe+O2![]() Fe3O4
Fe3O4
【答案】B
【解析】
A、化学反应遵循质量守恒定律,即反应前后各原子的数目和种类保持不变,该化学方程式中磷原子与氧原子的数目前后不一致,选项错误;
B、高锰酸钾在加热的条件下反应生成锰酸钾、二氧化锰和氧气,反应的化学方程式为2KMnO4![]() K2MnO4+MnO2+O2↑,选项正确;
K2MnO4+MnO2+O2↑,选项正确;
C、水在通电的条件下反应生成氢气和氧气,且生成的氢气和氧气均为气体,而该化学方程式中缺少反应条件,且氢气和氧气的化学式后面没有标气体符号,选项错误;
D、化学反应遵循质量守恒定律,即反应前后各原子的数目和种类保持不变,该化学方程式中铁原子与氧原子的数目前后不一致,选项错误,故选B。

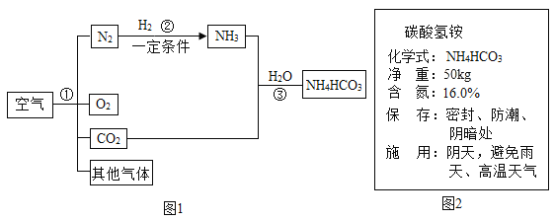
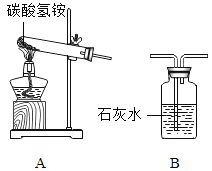
【题目】实验室中分别用高锰酸钾、过氧化氢、氯酸钾制取比较纯净的氧气。请你按照要求回答问题:
(1)结合图1所提供装置完成下列表格。
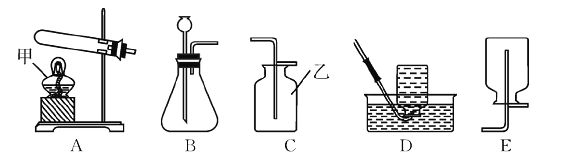
反应物填写内容 | 反应的文字表达式 | 气体制取装置组合(填序号) |
过氧化氢(二氧化锰) | 例:过氧化氢 | ____ |
高锰酸钾 | __________________ | ____ |
氯酸钾(二氧化锰) | _______________________ |
(2)请结合图1回答问题:
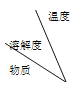
①写出甲、乙所指仪器名称:甲_____;乙_______;
②用过氧化氢制氧气的装置与其他两种方法的装置相比具有的优点是______、______ (写出两条);
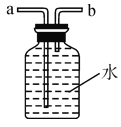
③若用图2装置收集一瓶氧气,气体应从______ (填“a”或“b”)端进入集气瓶。
(3)小柯为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见表。
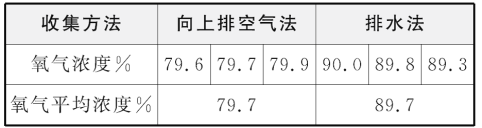
①小柯用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星木条复燃为氧气集满的标准;用排水法收集氧气时,以观察到______为氧气集满的标准。
②以上两种方法中,______法收集到的氧气更纯净。
③向上排空气法收集到的氧气浓度只有80%左右的原因有(_____)
A.氧气的密度略大于空气的密度
B.加热高锰酸钾固体产生氧气的浓度只有80%左右
C.当观察到带火星木条复燃时,集气瓶内还有空气
D.当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散
【题目】下表为氯化钠和硝酸钾部分溶解度,请根据表中数据填空。
| 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ |
| 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
①溶解度单位是________。
②称取40g粗盐(含少量不溶于水的杂质)进行提纯。20℃时,将其溶解,取水量最适合的是_______g(选填“100”“110”或“120”)。溶解、过滤、蒸发得到精盐,上述三步中都要用到的实验仪器是________。
③20℃时,将硝酸钾进行如下实验过程:进行A-D四个步骤
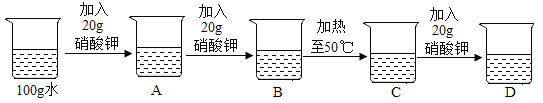
其中,C中为________(选填“饱和”“不饱和”)溶液,其中溶质质量分数最大的是________(选填A、B、C、D编号)。当D降温至10℃后,烧杯中得到硝酸钾固体________g,若要继续得到较多量的硝酸钾,易采用的结晶方法是_______(选填“蒸发”“降温”)。