题目内容
【题目】某无色气体可能含有CH4、H2、CO中的一种或几种,将该气体置于充满足量氧气的密闭容器中充分燃烧后,反应结束后测得容器中水和二氧化碳的质量比为9:11,则下列推断错误的是( )
A. 原无色气体可能是纯净的甲烷
B. 原无色气体可能是甲烷和氢气的混合气
C. 原无色气体可能是一氧化碳和氢气的混合气
D. 原气体中一定含有碳元素和氢元素
【答案】B
【解析】
反应结束后测得容器中水和二氧化碳的质量比为9:11,水中氢元素质量分数=![]() ,二氧化碳中碳元素的质量分数=
,二氧化碳中碳元素的质量分数=![]() ,所以生成物中碳元素和氢元素的质量比=
,所以生成物中碳元素和氢元素的质量比=![]() 。根据质量守恒可知,反应物中碳元素和氢元素的质量比=3:1;甲烷气体中C、H元素质量比=12:(1×4)=3:1,则混合气体中C、H元素质量比是3:1,因此可判断混合气体可能只有甲烷;也可能只含有CO和H2;也可能是甲烷、氢气、一氧化碳同时存在,不可能含有甲烷和另外任何一种气体。
。根据质量守恒可知,反应物中碳元素和氢元素的质量比=3:1;甲烷气体中C、H元素质量比=12:(1×4)=3:1,则混合气体中C、H元素质量比是3:1,因此可判断混合气体可能只有甲烷;也可能只含有CO和H2;也可能是甲烷、氢气、一氧化碳同时存在,不可能含有甲烷和另外任何一种气体。
根据地以上分析可知:
A、原无色气体可能是纯净的甲烷,故A正确;
B、原无色气体不可能是甲烷和氢气的混合气体,故B错误;
C、原无色气体可能是一氧化碳和氢气的混合气,故C正确;
D、原气体中一定含有碳元素和氢元素,故D正确。故选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】理科实验操作考试中有关于探究金属的某些物理性质和化学性质的试题,用坩埚钳夹取打磨过的铜片在酒精灯上加热,发现铜片表面变黑,为了探究黑色物质的成分。
(查阅资料)(1)铜的氧化物主要有两种:CuO(黑色);Cu2O(红色)
(2)酒精在不完全燃烧时会产生炭黑
(3)炭黑不与稀硫酸反应,也不溶于稀硫酸;氧化铜可与稀硫酸反应而溶解
(提出假设)猜想1:黑色物质为_____________。
猜想2:黑色物质为炭黑。
猜想3:黑色物质为_____________。
(设计方案)
操作步骤 | 实验中可能出现的现象 | 实验结论 |
取少量黑色固体于试管中,加入 足量___________(填物质名称) | ①_______ | 猜想1成立 |
② 黑色固体没有减少,溶液颜色不变 | 猜想2成立 | |
③_______ | 猜想3成立 |
(得出结论)通过实验现象,得出猜想3成立,此黑色固体为混合物。请写出实验中发生的化学方程式____________。
【题目】2016年1月1日,新的《环境空气质量标准》(简称AQI)正式实施,该标准严格规定了环境空气中SO2、NO2、PM10、PM2.5、O3(臭氧)和CO六类污染物的平均浓度。 具体限制数值如下表:
污染物项目 | PM2.5 | PM10 | SO2 | NO2 | CO | O3 | |
浓度限值 | 一级 | 35 | 40 | 20 | 40 | 4 | 100 |
二级 | 75 | 70 | 60 | 40 | 4 | 160 | |
单位 | g/m3 | mg/ m3 | g/m3 | ||||
为更好地治理大气环境,环保部门积极研究污染物变化特点,寻找变化规律,总结污染物随时间变化情况如图1所示。
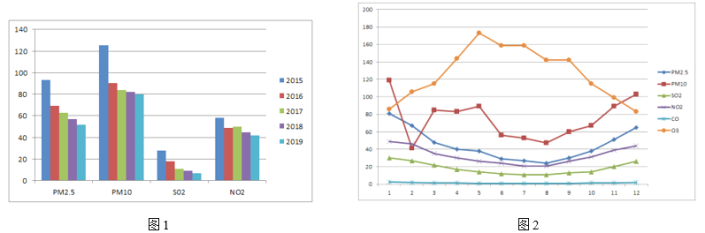
北京结合当地城市特点、污染物变化和季节气候特点,采取多项整治措施。对燃煤锅炉的能源进行改造,对平房进行“煤改电”改造、采取限行措施等。综合治理措施使得北京这样的北方超大型城市,在冬季供暖时节的污染物浓度得到有效控制。表2为2015-2018年第一季度,北京部分污染物平均浓度变化情况。
依据短文回答下列问题:
(1)主要污染物中属于单质的是_____。
(2)依据臭氧污染随时间变化的特点推测,影响臭氧污染发生的因素可能有____(至少答一点)。
(3)SO2形成酸雨过程如下图所示,该过程中化合价发生变化的元素有______。

(4)经过综合治理,北京地区污染物得到有效控制,并达到国家一级标准的是______。
(5)除文中提到的,你还知道的北京治理大气污染的措施有_____(答一条即可)。