题目内容
【题目】某化学兴趣小组的同学欲测定一瓶标签被腐蚀的盐酸浓度,将一定质量的盐酸滴加到装有25g石灰石样品的烧杯中(杂质不参与反应,也不溶于水),直到不在产生气泡为止。过滤,分别得到滤渣的质量5g和滤液质量111.2g。求:
(1)生成二氧化碳的质量是_________ g;
(2)所用盐酸的溶质质量分数_______。
【答案】8.8 14.6%
【解析】
解:参加反应的碳酸钙的质量为25g5g=20g
设参加反应的纯HCl的质量为x,生成的二氧化碳的质量为y
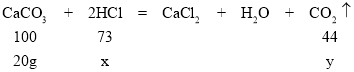
100:73=20g:x x=14.6g
100:44=20g:y y=8.8g
所用盐酸的质量为5g+111.2g+8.8g25g=100g
所用盐酸的溶质质量分数为![]() ×100%=14.6%
×100%=14.6%
答:(1)生成二氧化碳的质量是4.4g;(2)所用盐酸的溶质质量分数为14.6%。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】我校兴趣小组对废旧的干电池进行探究,同学们首先将干电池剖开发现有一层白色糊状物质,并闻到一股氨味。
(提出问题)白色糊状物的成分是什么?
(提供资料)
① 干电池的内部结构见如图,白色糊状物质A中除了含有淀粉,还含有一种盐,且该盐中阴离子是SO42-、CO32-、Cl-中的一种。
② 碘溶液能使淀粉变蓝。
③ 氨气可以使湿润的红色石蕊试纸变蓝。

(进行猜想)A中含有淀粉,A中的盐可能是铵盐。
(实验一)取少量A于试管中,滴加少量碘溶液,观察到_______________,证明A中含有淀粉。
(实验二)取少量A于研钵中,加入_____________固体,混合、研磨,产生刺激性气味的气体,该气体能使湿润的红色石蕊试纸变蓝,证明A中含有铵根离子。
(实验三)为了验证其阴离子的存在情况,兴趣小组再次设计如下实验,请你完成以下实验报告。
实验操作 | 实验现象 | 实验结论 |
(1)取糊状物少量,加足量的水,搅拌后过滤。取少量滤液于试管中,滴加氯化钡溶液。 | 无现象 | ________________ |
(2)另取第(1)步所得滤液少量,滴加少量_____________溶液 | 产生白色沉淀 | 存在的离子是Cl- |
(得出结论)上述实验证明,电池内白色糊状物含有淀粉和氯化铵两种物质。
(反馈交流)兴趣小组指导老师指出实验三的方案设计存在错误,请你说明错误的原因并将其改正:___________________________。
(知识应用)回收废旧干电池不仅可以减少环境污染,还能变废为宝。根据上述探究过程,请简要说明干电池中的白色糊状物的回收价值有:__________________________________。