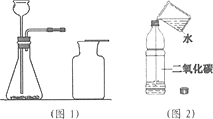
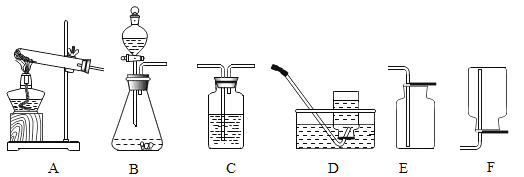
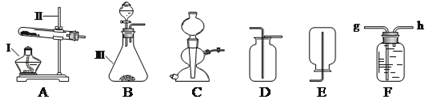题目内容
【题目】化学小组发现,铜制品表面出现了绿色物质,于是想探究绿色物质产生的条件。
查阅资料:铜在空气中会生锈,铜锈为绿色物质,俗称“铜绿”,主要成分是Cu2(OH)2CO3;
【猜想】
小组同学经讨论,做出以下两个合理的猜想:
猜想一:铜生锈只与空气中的H2O和气体X有关,则气体X是________。
猜想二:铜生锈只与空气中的H2O、气体X和气体Y有关,则气体Y是_______。
上述猜想的理由是_______。
【实验】
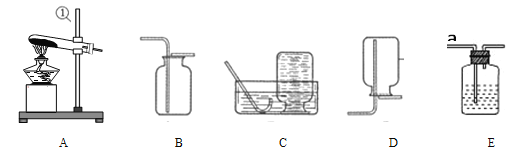
小组同学设计并进行了右图所示的实验。
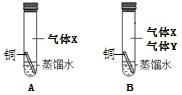
现象:一段时间后,观察到A试管中的铜丝无明显变化, B试管中的铜丝出现铜锈,多次实验均得到同样的结果。
【结论】
铜生锈的是铜与空气中的_______共同作用的结果。
【拓展】
(1)实验需使用经煮沸迅速冷却的蒸馏水,原因是_________;
(2)除去铜锈可用稀盐酸,写出铜锈与稀盐酸反应的化学方程式__________。
【答案】 CO2 O2 因为Cu2(OH)2CO3中含有C、H、O等元素,根据质量守恒定律,
铜生锈必须有含C、H、O元素的物质参与 H2O 、CO2 、O2 除去蒸馏水中溶解的空气 Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑
【解析】(1)铜绿的化学式为Cu2(OH)2CO3;根据质量守恒定律,由化学式可知,铜生锈需要与空气中的水和二氧化碳和氧气接触;因为Cu2(OH)2CO3中含有C、H、O等元素,根据质量守恒定律,铜生锈必须有含C、H、O元素的物质参与;
(2)由实验可知,铜生锈与空气中的水、二氧化碳、氧气接触;
(3)煮沸迅速冷却的蒸馏水可以除去蒸馏水中溶解的空气,从而除去了对实验的影响;铜锈与稀盐酸反应生成氯化铜、二氧化碳和水,反应方程式为Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑;