题目内容
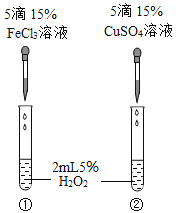
【题目】为比较Fe3+和Cu2+对过氧化氢分解反应的催化效果,某同学设计了如图所示的实验(FeCl3溶液、CuSO4溶液中都含有阴阳离子和水分子),有关实验有如下说法:
①过氧化氢中氧元素的化合价为-1价;
②若图1所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好;
③实验中可通过观察产生气泡快慢来比较反应速率;
④滴加FeCl3或CuSO4溶液后过氧化氢分解速率加快,则FeCl3或CuSO4是过氧化氢催化剂
以上说法不正确的是( )
A.①②B.①④C.②④D.③④
【答案】C
【解析】
①过氧化氢中氢显+1价,根据化合物中元素化合价之和为零,可知氧元素的化合价为-1价,故①正确;
②因二者所含的阴离子不同,要证明Fe3+比Cu2+对H2O2分解催化效果好,还要使选择的试剂中阴离子种类相同,故②错误;
③反应的剧烈程度与实验现象有关,反应越剧烈,产生气体的速率越快,产生气泡越快,故③正确;
④证明氯化铁或硫酸铜是过氧化氢分解的催化剂,还需要验证质量和化学性质不变,故④错误。所以说法不正确的是②④。故选C。

 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
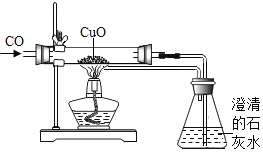
各地期末复习特训卷系列答案【题目】某化学兴趣小组对“氧化铜能否作过氧化氢分解的催化剂“进行了探究
(实验探究)
实验编号 | 实验操作 | 实验现象 | 实验分析或结论 | |
实验分析 | 实验结论 | |||
① |
| 有少量气泡;木条不复燃 | 过氧化氢能分解,但是 _________ | 氧化铜是过氧化氢分解的催化剂 |
② |
| __________________ | 氧化铜能加快过氧化氢分解 | |
(1)写出实验②中反应的化学方程式:___________________。
(交流反思)实验过程中加入到两支试管里的过氧化氢溶液应满足的要求有_________________。
①体积相同 ②浓度相同 ③温度相同
(2)小明同学认为仅由上述实验还不能完全得出表内的“总结”,他补充设计了以下两个探究实验
实验一:称量反应后固体质量,并与反应前的称量数据作比较,其目的是________________。
实验二:另取5mL5%的过氧化氢溶液于试管中,再向其中加入实验②反应后的固体剩余物,如图1所示,其目的是证明_______________________。
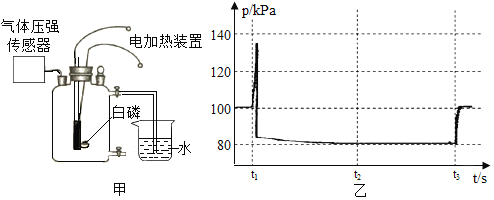
(实验拓展)小红同学用MnO2、CuO两种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球探究分解过氧化氢溶液制取氧气的适宜催化剂。
实验操作:取30粒含MnO2的海藻酸钠微球,采用图1装置进行实验。改用另一种微球,分别重复上述实验,得到图2的锥形瓶内压强随时间变化的曲线图。
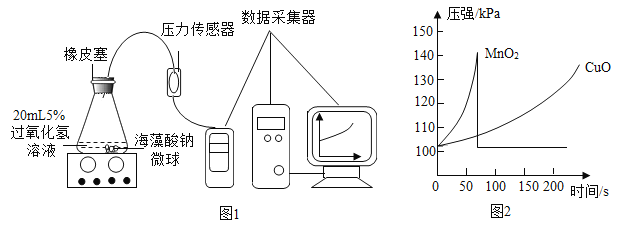
(3)每次实验时,海藻酸钠微球数应相同的原因是_____________。
(4)用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是_______________。
(5)从实验曲线看,催化效果较好、反应温和的催化剂是__________________。
【题目】结合下表给出的![]() 和
和![]() 的溶解度,回答下列问题:
的溶解度,回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g |
| 13.3 | 31.6 | 63.9 | 110 | 169 | 245 |
| 35.7 | 36.0 | 35.6 | 37.3 | 38.4 | 33.8 | |
(1)20℃时,将40g ![]() ,加入100g水中,所得溶液的质量为_____g;
,加入100g水中,所得溶液的质量为_____g;
(2)这两种物质中溶解度受温度变化影响较小的是_____;
(3)将90g ![]() 和30g
和30g![]() 组成的混合物放入100g60℃的水中充分搅拌,当温度降低到20℃时,发现有较多固体析出,下列说法中,正确的是_____。
组成的混合物放入100g60℃的水中充分搅拌,当温度降低到20℃时,发现有较多固体析出,下列说法中,正确的是_____。
A 析出的固体是![]() B 剩余的母液中含有
B 剩余的母液中含有![]() 和
和![]() 两种溶质
两种溶质