题目内容
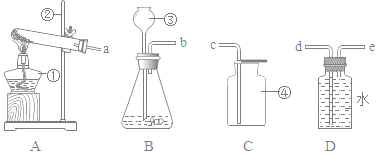
【题目】(1)某实验小组的同学用碳酸钠粉末、块状大理石、稀盐酸、稀硫酸这几种药品,探究哪两种药品的反应适合在实验室制取C02。请你参与下列的探究并回答问题:
(提出问题)上述酸和碳酸盐的反应是否适合在实验室制取C02?
Ⅰ.设计了如下三个实验进行对比
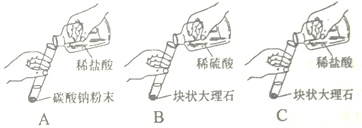
(实验与结论)
Ⅱ.请你填写实验报告
实验 | 实验现象 | 实验内容 |
A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,不便收集气体,不宜于实验室制取二氧化碳 |
B | 产生气泡,速率迅速减慢,反应几乎停止 | 无法持续产生二氧化碳,不能用于实验室制取二氧化碳 |
C | ①______; | ②______; |
Ⅲ.根据探究结论,实验室制取二氧化碳的反应原理为______(用化学方程式表示)
(2)取四朵用石蕊溶液染成紫色的干燥纸花完成如下实验。
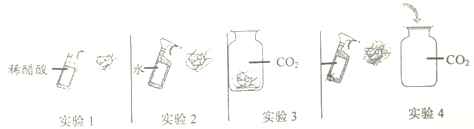
①该同学进行的实验1、2两项实验说明了酸能使紫色石蕊溶液变红;则该同学进行的实验3、4两项实验说明了______。
②写出实验4中发生反应的化学方程式:______。
③若将第四朵小花取出,小心烘烤,可观察到的现象是______。
【答案】产生大量气泡 反应速率适中,便于收集气体 CaCO3+2HCl==CaCl2+H2O+CO2↑ 二氧化碳与水反应生成酸(或碳酸) CO2+H2O==H2CO3 变红色的纸花又变成紫色
【解析】
本题主要考查实验室制取二氧化碳药品的选择和二氧化碳的化学性质。
(1)稀盐酸和大理石反应是实验室制取二氧化碳的方法,稀盐酸和大理石中的碳酸钙反应能够产生大量气泡,速率适中且持久,便于收集,因此适用于实验室制取二氧化碳,故答案为:产生大量气泡;
(2)由(1)的分析可知,实验内容为:反应速率适中,便于收集气体,故答案为:反应速率适中,便于收集气体;
(3)稀盐酸和大理石反应产生氯化钙、水和二氧化碳,因此反应的原理为:CaCO3+2HCl=CaCl2+H2O+CO2↑,故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)二氧化碳本身不显酸性,不能使石蕊变色,与水反应生成的碳酸显酸性,能使石蕊变红;故答案为:二氧化碳与水反应生成酸(或碳酸);
(5)二氧化碳能与水反应生成碳酸,反应化学方程式为:CO2+H2O=H2CO3,故答案为:CO2+H2O=H2CO3;
(6)碳酸不稳定,受热易分解生成二氧化碳和水,使酸性消失,因此花由红色变为紫色,故答案为:变红色的纸花又变成紫色。

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案【题目】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究.
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1:不相等;猜想2:相等.
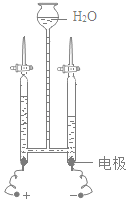
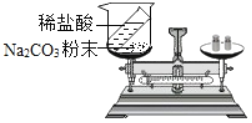
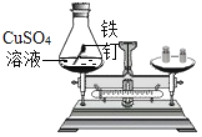
(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量.
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
实验现象 | 有气泡产生 天平指针向右偏转 | 铁钉表面有红色物质析出,天平指针没有偏转 |
结论 | 猜想1正确 | 猜想2正确 |
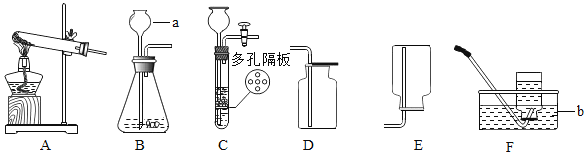
(反思评价)经过反复讨论最后得出:在探究化学反应前后各物质的质量总和是否相等时,凡有气体参加或生成的反应,都应在_____中进行.
(优化装置)同学们对甲组左盘中的反应装置进行了如图所示的三种改进.经过反复交流,一致认为:A的改进会因_____从而产生误差;B的改进会因反应产生气体使瓶内压强太大,使塞子蹦出而产生危险;C的改进最为科学,那么C的锥形瓶中盛放的NaOH溶液的作用是_____.
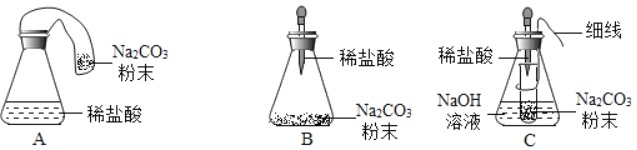
(得出结论)利用C装置进行再次探究,均得出猜想2正确的结论.
进一步分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论:_____的各物质的质量总和等于反应后生成的各物质的质量总和.
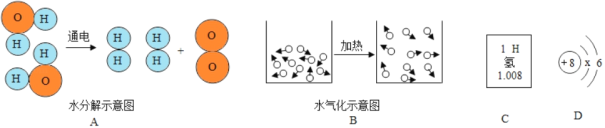
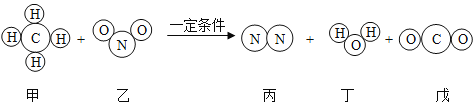
(微观解释)化学反应前后,_____均不变,所以质量守恒.
(应用)某固体物质受热发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由_____组成.