题目内容
【题目】氮元素有多种化合价,也能形成多种常见的物质。如:N2、NH4Cl、N2O3、NO2、NO等。试回答相关问题:
(1)将上述五种含氮物质按氮元素化合价由高到低排列_____。
(2)氮气(N2)的相对分子质量为_____。
(3)氯化铵(NH4Cl)中各元素的质量比为_____。
(4)计算五氧化二氮(N2O5)中氮元素的质量分数(精确到0.1%)。_____
【答案】NO2、N2O3、NO、N2、NH4Cl 28 28:8:71 26.0%
【解析】
(1)N2中氮元素为0价,NH4Cl中氮元素为﹣3价,N2O3中氮元素为+3价,NO2中氮元素为+4价,NO中氮元素为+2价,将上述五种含氮物质按氮元素化合价由高到低排列NO2、N2O3、NO、N2、NH4Cl。
(2)氮气(N2)的相对分子质量为 14×2=28。
(3)氯化铵(NH4Cl)中氮、氢、氯元素的质量比为 14:(1×4):35.5=28:8:71。
(4)五氧化二氮(N2O5)中氮元素的质量分数为![]() ×100%≈26.0%
×100%≈26.0%
故答案为:
(1)NO2、N2O3、NO、N2、NH4Cl。(2)28。(3)28:8:71。(4)26.0%

 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案【题目】(1)某实验小组的同学用碳酸钠粉末、块状大理石、稀盐酸、稀硫酸这几种药品,探究哪两种药品的反应适合在实验室制取C02。请你参与下列的探究并回答问题:
(提出问题)上述酸和碳酸盐的反应是否适合在实验室制取C02?
Ⅰ.设计了如下三个实验进行对比
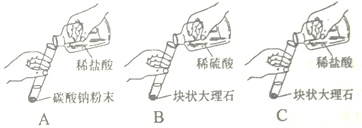
(实验与结论)
Ⅱ.请你填写实验报告
实验 | 实验现象 | 实验内容 |
A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,不便收集气体,不宜于实验室制取二氧化碳 |
B | 产生气泡,速率迅速减慢,反应几乎停止 | 无法持续产生二氧化碳,不能用于实验室制取二氧化碳 |
C | ①______; | ②______; |
Ⅲ.根据探究结论,实验室制取二氧化碳的反应原理为______(用化学方程式表示)
(2)取四朵用石蕊溶液染成紫色的干燥纸花完成如下实验。
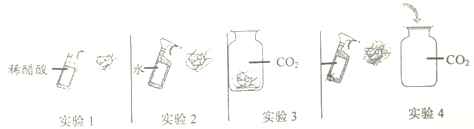
①该同学进行的实验1、2两项实验说明了酸能使紫色石蕊溶液变红;则该同学进行的实验3、4两项实验说明了______。
②写出实验4中发生反应的化学方程式:______。
③若将第四朵小花取出,小心烘烤,可观察到的现象是______。