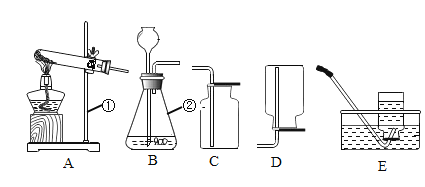
题目内容
【题目】实验室有失去标签的五个试剂瓶,分别盛有NaOH溶液、CuSO4溶液、BaCl2溶液、稀盐酸和稀硫酸。鉴别操作如下:
(1)呈蓝色的溶液为CuSO4溶液。取少量其他溶液分别于四支试管中,再分别滴加CuSO4溶液,可鉴别出NaOH溶液和BaCl2溶液。鉴别出NaOH溶液的现象是_____。
(2)另取少量剩余的两种溶液分别放入两支试管中,再分别滴加BaCl2溶液,其中一支试管内产生白色沉淀,该反应的化学方程式为_____。
(3)实验结束后,将所有试管中的物质充分混合,过滤除去沉淀,得到无色滤液,此滤液一定含有的溶质为_____(填化学式)。取少量无色滤液滴加Na2SO4溶液,无明显现象。另取少量无色滤液分别与下列物质混合时,一定无明显现象的是_____。
A Ba(OH)2溶液 B AgNO3溶液 C Mg D 酚酞溶液
【答案】产生蓝色沉淀 ![]()
![]() C
C
【解析】
(1)呈蓝色的溶液为CuSO4溶液。取少量其他溶液分别于四支试管中,再分别滴加CuSO4溶液,可鉴别出NaOH溶液和BaCl2溶液。CuSO4溶液与BaCl2溶液产生白色沉淀;CuSO4溶液与NaOH溶液产生蓝色沉淀;鉴别出NaOH溶液的现象是产生蓝色沉淀;故填:产生蓝色沉淀
(2)另取少量剩余的两种溶液分别放入两支试管中,再分别滴加BaCl2溶液,能与BaCl2溶液产生白色沉淀的是稀硫酸,其反应的化学方程式为:H2SO4+ BaCl2 ==BaSO4![]() +2HCl;故填:H2SO4+ BaCl2 ==BaSO4
+2HCl;故填:H2SO4+ BaCl2 ==BaSO4![]() +2HCl
+2HCl
(3)根据反应可知,氯化钠为反应产物,且可溶解在水里,故此滤液一定含有的溶质为NaCl;
将五种溶液混合,过滤后得到无色溶液,说明铜元素全在氢氧化铜沉淀里,滤液里无铜离子,试管中能生成氢氧化铜沉淀,说明滤液中没有氢离子,滤液加入硫酸钠后没有明显现象,说明滤液中没有钡离子。
A、溶液中可能含有硫酸根离子,因此加入氢氧化钡后可能有沉淀生成,故不符合题意;
B、溶液中含有氯离子,因此加入硝酸银后有沉淀生成,故不符合题意;
C、溶液中没有氢离子,因此加入镁后没有明显现象,故符合题意;
D、根据以上分析可知滤液中没有氢离子,滤液呈碱性或中性,所以加入酚酞可能会有明显现象,故不符合题意;
故填C

 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案【题目】某兴趣小组同学对实验室制取氧气的催化剂进行如下探究:
(提出问题)二氧化锰常作为氯酸钾分解制取氧气的催化剂,其他氧化物是否也能催化氯酸钾分解呢?
(查阅资料)研究表明,许多金属氧化物对氯酸钾的分解(分解时放出热量)有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
氧化铁 | 氧化铝 | 氧化铜 | 氧化镁 | |
开始反应(℃) | 420 | 515 | 305 | 490 |
剧烈反应(℃) | 490 | 540 | 350 | 545 |
(1)实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用的金属氧化物是_____。
(设计并完成实验)Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰混合均匀加热
Ⅲ.将Xg氯酸钾与1.0g氧化铜混合均匀加热
(2)实验Ⅲ中X的值应为_____,实验_____和Ⅲ比较可证明氧化铜能加快氯酸钾的分解速率。
(实验现象分析)将实验Ⅲ反应后的固体加水溶液、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和Xg氯酸钾混合加热,现象与实验Ⅲ相同。
(3)在相同温度下比较两组实验产生氧气的快慢,通常可采用的方法有_____。
(结论)氧化铜也能做氯酸钾分解的催化剂。
(4)实验Ⅲ反应的文字表达式为_____。
注意:若答对第(5)小题奖励4分,化学试卷总分不超过60分。
(5)氯酸钾分解制取氧气的快慢还与哪些因素有关?请你提出新的合理的假设和实验方案。
(假设)_____。
(实验方案)_____。
(结论)_____。