题目内容
【题目】下图中的A~F是初中化学实验中常用的几种装置,按要求回答问题。
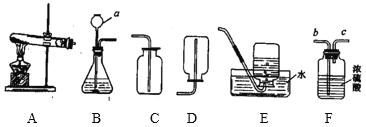
(1)写出仪器a的名称:_____。
(2)若实验室用高锰酸钾制取氧气,应选用的发生装置为_____,该反应的化学方程式为_____。
(3)若实验室用大理石和稀盐酸制取并收集二氧化碳,应选用的装置为_____,该反应的化学方程式为_____。把生成的气体从_____(填“b”或“e”)通入F装置,可得到干燥的二氧化碳气体。
(4)往试管里装入固体粉末时,可先使试管倾斜,把盛有药品的药匙小心地送至试管_____(“上部”、“中部”或“底部”),然后使试管直立起来。
【答案】长颈漏斗 A ![]() BC
BC ![]() b 底部
b 底部
【解析】
(1)由图可知仪器a是长颈漏斗:故填:长颈漏斗
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,实验室用高锰酸钾制取氧气,可选用的发生装置为A,高锰酸钾加热分解生成氧气,化学方程式为:2KMnO4![]() K2MnO4+ MnO2+O2
K2MnO4+ MnO2+O2![]() ;故填:A;2KMnO4
;故填:A;2KMnO4![]() K2MnO4+ MnO2+O2
K2MnO4+ MnO2+O2![]()
(3)实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳的密度比空气大,溶于水,所以用大理石和稀盐酸制取并收集二氧化碳,可选用的发生及收集装置是BC,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl==CaCl2 +H2O+ CO2![]() ;把生成的气体通入浓硫酸干燥时,应该长进短出,让气体与浓硫酸充分接触,从b通入F装置,可得到干燥的二氧化碳气体。故填:BC;CaCO3+2HCl==CaCl2 +H2O+ CO2
;把生成的气体通入浓硫酸干燥时,应该长进短出,让气体与浓硫酸充分接触,从b通入F装置,可得到干燥的二氧化碳气体。故填:BC;CaCO3+2HCl==CaCl2 +H2O+ CO2![]() ;b
;b
(4)往试管里装入固体粉末时,可先使试管倾斜,把盛有药品的药匙小心地送至试管底部,然后使试管直立起来,防止固体粉末附在试管壁上。故填:底部

练习册系列答案
相关题目