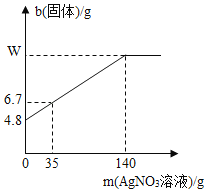
��Ŀ����
����Ŀ��ʵ������һЩ�����Ͷ�����̼�Ļ�����壬Ϊ���������Ƿ������CO��ͬѧ�ǽ���������ʵ�飺
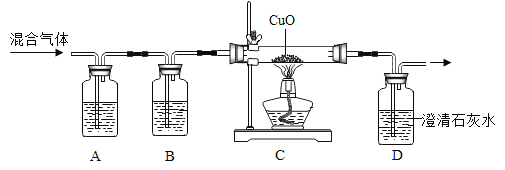
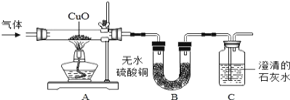
�������ϣ��������л�ԭ�ԣ�������������������ͭ��Ӧ����ͭ��ˮ��
��ش���������
��1��С��ͬѧ˵Cװ��������ͭ��ɺ�ɫ���壬��֤����CO������ΪC�з�Ӧ��ѧ����ʽΪ_______________��
��2����С�Ƹ������Ϊ����Ҳ�ܷ������Ʒ�Ӧ�������Ӧ�۲쵽D�б���ǣ���֤����CO��D�з�Ӧ��ѧ����ʽΪ____________________��
��3����СΰҲ���D�б���ǻ�������֤������������е�CO2Ҳ����������������A��װ����������ʯ��ˮ��B��װ������ʯ��ˮ����װ��A��������_______________��װ��B��������______________________��
��4������ͬѧ��һ����ͬСΰ����ƣ����ڼ�������У����۲쵽____________����ʱ������֤����������к���CO��
��5������ʵ��β����һ�ִ���������__________________________________________��
���𰸡�CO+CuO![]() Cu+CO2 CO2+Ca��OH��2�TCaCO3��+H2O ��ȥ������̼ ���������̼�Ƿ���ɾ� B��ʯ��ˮ������ǣ�D��ʯ��ˮ����� �ڳ����ڴ�����һȼ�ŵľƾ��ƣ���δ��Ӧ��һ����̼�յ����������ɣ�
Cu+CO2 CO2+Ca��OH��2�TCaCO3��+H2O ��ȥ������̼ ���������̼�Ƿ���ɾ� B��ʯ��ˮ������ǣ�D��ʯ��ˮ����� �ڳ����ڴ�����һȼ�ŵľƾ��ƣ���δ��Ӧ��һ����̼�յ����������ɣ�
��������
��ʵ�������ǣ�Aװ���������ջ�������еĶ�����̼����B������ǣ���֤����������еĶ�����̼��������ȫ����B�г����������ʣ��������һ����̼�����Ƕ���������ͭ������Ӧ������������ͭ��Ӧ����ˮ����һ����̼������ͭ��Ӧ���ɶ�����̼��������̼����ʹD�г��ֻ�������ֻҪD�б���Ǿ�֤�������������һ����̼��
��1��һ����̼���л�ԭ�ԣ��ڼ���ʱ��������ͭ��Ӧ��С��ͬѧ˵Cװ��������ͭ��ɺ�ɫ���壬��֤����CO��C�з�Ӧ��ѧ����ʽΪ��CO+CuO![]() Cu+CO2��
Cu+CO2��
��2�����ڶ�����̼�����������Ʒ�Ӧ������̼��ƺ�ˮ������D�з�Ӧ��ѧ����ʽΪ��CO2+Ca��OH��2�TCaCO3��+H2O��
��3�����ڶ�����̼�����������Ʒ�Ӧ������̼��ƺ�ˮ��ʵ���Ҽ���һ����̼ͨ���ǽ�һ����̼ת��Ϊ������̼��Ȼ�����ó���ʯ��ˮȥ���������̼�����û��������ԭ�����ж�����̼��Ϊ�˱���������ţ�����Ӧ���ȰѶ�����̼�����꣬��Aװ��Ŀ�ľ��dz�ȥ������̼��Bװ�����������������ж�����̼�Ƿ�������ȫ��
��4���ڼ�������У����۲쵽A��ʯ��ˮ����ǣ�B�л�ˮ������ǣ�D��ʯ��ˮ���������ʱ������֤����������к���CO��
��5������β���к���һ����̼������Ⱦ���������п�ȼ�ԡ���������ʵ��β����һ�ִ��������ǣ��ڳ����ڴ�����һȼ�ŵľƾ��ƣ���δ��Ӧ��һ����̼ȼ�յ���