题目内容
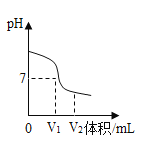
【题目】小黄同学为了测定某Cu﹣Ag合金中各金属的含量,取这种合金4.8 g与AgNO3溶液反应,加入AgNO3溶液的质量m与充分反应后所得固体的质量b的关系如图所示.请计算:
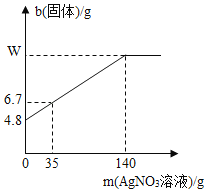
(1)AgNO3溶液中溶质的质量分数(结果精确 至0.1%);
(2)该合金中银和铜的质量比(结果精确至0.1).
【答案】(1)12.1%(2)2:1
【解析】
解:(1)6.7g-4.8g=1.9g,设35gAgNO3溶液中含AgNO3的质量为x,则有:
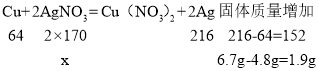
![]()
x=4.25g
硝酸银溶液中溶质的质量分数=![]() ×100%
×100%![]() 12.1%;
12.1%;
答:硝酸银溶液中溶质的质量分数为12.1%。
(2)140gAgNO3溶液中溶质的质量为140g×12.1%=17g
设4.8gCu﹣Ag合金中Cu的质量为y,
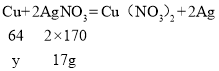
![]()
解得y=3.2g
m(Ag)=4.8g﹣3.2g=1.6g
m(Cu):m(Ag)=3.2g:1.6g=2:1
答:该合金中铜与银的质量比为 2:1.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案
相关题目
【题目】Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组的同学为了测定某黄铜的组成,取20g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于如表:
加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) | |
第1次 | 20 | 17.4 |
第2次 | 20 | 14.8 |
第3次 | 20 | 12.2 |
第4次 | 20 | 12 |
第5次 | 20 | m |
试回答下列问题:
(1)上述表格中m的值为_____;
(2)黄铜样品中锌的质量为_____;
(3)所用稀硫酸中硫酸的质量分数是_____。