题目内容
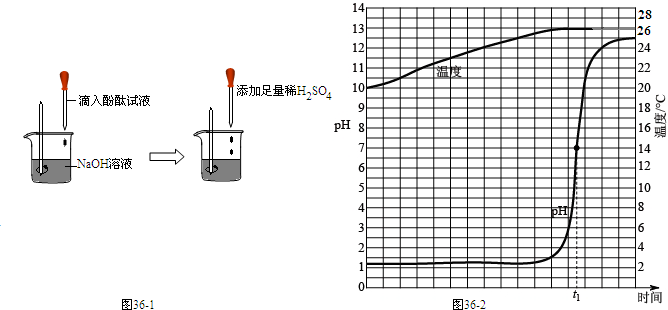
在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应.请与他们一起完成实验方案设计、实施和评价.(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(常温下)他们先测定出某NaOH溶液的pH 7(填“大于”、“等于”或“小于”),然后将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后再测定其pH,发现其pH小于7.
结论:稀H2SO4与NaOH溶液发生了化学反应,并且 过量.
(2)方案二:利用酸碱指示剂
①探究稀H2SO4与NaOH溶液的反应
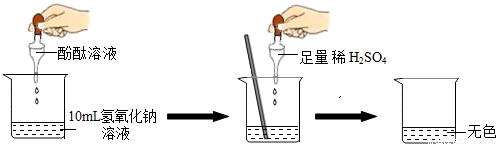
如图所示进行实验.当滴入几滴酚酞溶液后,溶液由无色变为 色.根据上述过程中的颜色变化,确定稀H2SO4与NaOH溶液发生了反应,该反应的化学方程式为 .
②探究上述稀H2SO4与NaOH溶液反应后烧杯中的硫酸是否过量
根据上述反应过程中溶液变成无色,不能确定稀H2SO4是否过量,同学们又分别选取BaCl2溶液与、紫色石蕊溶液、Na2CO3粉末设计实验方案,请你判断并分析:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的BaCl2溶液 | 出现白色沉淀 | 稀H2SO4过量 |
| 方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 稀H2SO4过量 |
| 方案三 | 取样,加入Na2CO3粉末 | 有气体产生 | 稀H2SO4过量 |
【答案】分析:硫酸和氢氧化钠的反应,两者是否完全反应是存在三种可能的,而题目限定在恰好完全反应和硫酸过量的两种情况下的,所以只需要关注硫酸是否有剩余即可.当硫酸剩余时,既可以借助测定溶液的pH值,也可以借助酸的通性来进行,其实质都是检测氢离子或者消耗氢离子.
解答:解:(1)硫酸和氢氧化钠溶液的pH值,硫酸的pH小于7,氢氧化钠的pH大于7.当混合后,测定其pH小于7时,说明溶液显酸性,即硫酸有剩余.
(2)当借助酸碱指示剂
①图中给出的实验的第一步是向氢氧化钠溶液中滴入了酚酞,所以滴入酚酞后的颜色变化是由无色变红红色(酚酞遇碱变红).第二步是滴入适量的硫酸,溶液会由红色变成无色,证明碱被慢慢消耗,从而证明酸和碱发生了反应,氢氧化钠和硫酸发生的是中和反应生成对应的硫酸钠和水,对应方程式为2NaOH+H2SO4═Na2SO4+2H2O.
②对于硫酸是否过量的判断实际上是判断溶液中是否依然显酸性.
方案三中反应的化学方程式为 Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.上述设计的实验方案中,不正确的是 方案一.错误的原因是即使硫酸不过量,先前生成的硫酸钠也能和氯化钡反应生成白色沉淀(或者:反应是通过生成沉淀来进行分析氢离子是否剩余的,而沉淀硫酸钡的生成与氢离子无关,所以不能确定是否硫酸过量)
其他的证明硫酸过量的方法可以使用氧化铜、氧化铁等不溶性金属氧化物或者不溶性氢氧化物氢氧化铜或者氢氧化铁等,观察是否能够溶解以及颜色变化.
故答案为:(1)大于; 稀硫酸.
(2)①红; 2NaOH+H2SO4═Na2SO4+2H2O.②Na2CO3+H2SO4═Na2SO4+H2O+CO2↑;方案一; 即使硫酸不过量,先前生成的硫酸钠也能和氯化钡反应生成白色沉淀(或者:反应是通过生成沉淀来进行分析氢离子是否剩余的,而沉淀硫酸钡的生成与氢离子无关,所以不能确定是否硫酸过量;加入氧化铜,观察溶液的颜色变化,若显示为蓝色,则硫酸过量(其余合理即可)
点评:注意从题目限制的环境下进行实验的设计,这样能够避免设计中出现的过多的情况的考虑,从而降低题目的难度.
解答:解:(1)硫酸和氢氧化钠溶液的pH值,硫酸的pH小于7,氢氧化钠的pH大于7.当混合后,测定其pH小于7时,说明溶液显酸性,即硫酸有剩余.
(2)当借助酸碱指示剂
①图中给出的实验的第一步是向氢氧化钠溶液中滴入了酚酞,所以滴入酚酞后的颜色变化是由无色变红红色(酚酞遇碱变红).第二步是滴入适量的硫酸,溶液会由红色变成无色,证明碱被慢慢消耗,从而证明酸和碱发生了反应,氢氧化钠和硫酸发生的是中和反应生成对应的硫酸钠和水,对应方程式为2NaOH+H2SO4═Na2SO4+2H2O.
②对于硫酸是否过量的判断实际上是判断溶液中是否依然显酸性.
| 实验方案 | 实验步骤 | 实验现象及反应方程式 | 实验分析 |
| 方案一 | BaCl2溶液 | 出现白色沉淀 H2SO4+BaCl2=BaSO4↓+2HCl;Na2SO4+BaCl2=BaSO4↓+2NaCl | 反应是通过生成沉淀来进行分析氢离子是否剩余的,而沉淀硫酸钡的生成与氢离子无关,所以不能确定是否硫酸过量 |
| 方案二 | 紫色石蕊溶液 | 溶液变红 | 紫色石蕊遇到酸性溶液变红,所以通过石蕊变红这一点可以证明氢离子的存在,进而确定硫酸是过量的. |
| 方案三 | Na2CO3粉末 | 有气体产生 Na2CO3+H2SO4═Na2SO4+H2O+CO2↑ | 碳酸钠遇到酸能够反应生成二氧化碳气体,所以加入碳酸钠生成气体时,能够证明溶液显酸性,即稀H2SO4过量 |
其他的证明硫酸过量的方法可以使用氧化铜、氧化铁等不溶性金属氧化物或者不溶性氢氧化物氢氧化铜或者氢氧化铁等,观察是否能够溶解以及颜色变化.
故答案为:(1)大于; 稀硫酸.
(2)①红; 2NaOH+H2SO4═Na2SO4+2H2O.②Na2CO3+H2SO4═Na2SO4+H2O+CO2↑;方案一; 即使硫酸不过量,先前生成的硫酸钠也能和氯化钡反应生成白色沉淀(或者:反应是通过生成沉淀来进行分析氢离子是否剩余的,而沉淀硫酸钡的生成与氢离子无关,所以不能确定是否硫酸过量;加入氧化铜,观察溶液的颜色变化,若显示为蓝色,则硫酸过量(其余合理即可)
点评:注意从题目限制的环境下进行实验的设计,这样能够避免设计中出现的过多的情况的考虑,从而降低题目的难度.

练习册系列答案
相关题目