题目内容
【题目】通过化学的学习,小明同学感悟到学习化学开拓了思维,增长了智慧.
(1)将宏观、微观和符号表征相结合是化学独特的思维方式;
科学家最近在低温下合成了一种化合物,其分子模型如图所示,其中“ ![]() ”代表碳原子,“
”代表碳原子,“ ![]() ”代表氢原子.请补充该物质燃烧的化学方程式: .
”代表氢原子.请补充该物质燃烧的化学方程式: . 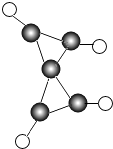
(2)化学的学习使人们认识了物质的变化规律,并以此为依据,寻找到制取物质的方法:
①电解是控制反应条件使物质发生某种变化而产生新物质的方法.人们可以利用电解食盐水来制取烧碱,电解食盐水生成烧碱的同时还会产生氯气(Cl2)和氢气两种气体.写出该反应的化学方程式: . 从原料选择依据的角度看,氯化钠之所以可作制烧碱的原料是因为氯化钠中含有 .
②根据所制物质的组成成分选择原料,要考虑原料中能否提供所得产品中所需的成分且能够转化到产品中:如海水制“碱”中,NaCl只提供了Na2CO3所需的“Na”,则还需要能提供含元素的物质.按此思路,用Na2CO3制取NaOH,需要用到生活中常见的一种廉价原料是(填俗称),从经济角度考虑该变化体现了“化学变化创造价值”.
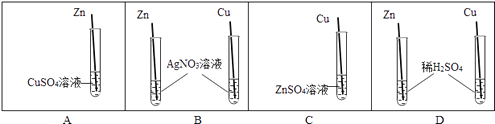
③已知由Cu到Cu(OH)2可经三步转化:Cu→CuO→CuSO4→Cu(OH)2 , 而Fe经两步反应可得到Fe(OH)2 , 请补全转化的过程:Fe→→Fe(OH)2 .
【答案】
(1)C5H4+6O2 ![]() 5CO2+2H2O
5CO2+2H2O
(2)2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑;钠元素;碳、氧;熟石灰;FeCl2
2NaOH+H2↑+Cl2↑;钠元素;碳、氧;熟石灰;FeCl2
【解析】解:(1)由一种化合物的分子模型图可知,1个该化合物的分子是由5个碳原子和4个氢原子构成的,则该化合物的化学式为C5H4;燃烧生成二氧化碳和水,反应的化学方程式为C5H4+6O2 ![]() 5CO2+2H2O.
5CO2+2H2O.
所以答案是:C5H4 , 2H2O.(2)①电解食盐水生成烧碱的同时还会产生氯气(Cl2)和氢气两种气体,该反应的化学方程式:2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑,从原料选择依据的角度看,氯化钠之所以可作制烧碱的原料是因为氯化钠中含有钠元素.②由质量守恒定律可知,海水制“碱”中,NaCl只提供了Na2CO3所需的“Na”,则还需要能提供含碳、氧元素的物质,按此思路,用Na2CO3制取NaOH,需要用到生活中常见的一种廉价原料是熟石灰,从经济角度考虑该变化体现了“化学变化创造价值”.③要将Fe经两步反应可得到Fe(OH)2 , 可以将铁与盐酸等反应生成氯化亚铁,再与碱溶液反应即可,所以,转化的过程是:Fe→FeCl2→Fe(OH)2 . 所以答案是:①2NaCl+2H2O
2NaOH+H2↑+Cl2↑,从原料选择依据的角度看,氯化钠之所以可作制烧碱的原料是因为氯化钠中含有钠元素.②由质量守恒定律可知,海水制“碱”中,NaCl只提供了Na2CO3所需的“Na”,则还需要能提供含碳、氧元素的物质,按此思路,用Na2CO3制取NaOH,需要用到生活中常见的一种廉价原料是熟石灰,从经济角度考虑该变化体现了“化学变化创造价值”.③要将Fe经两步反应可得到Fe(OH)2 , 可以将铁与盐酸等反应生成氯化亚铁,再与碱溶液反应即可,所以,转化的过程是:Fe→FeCl2→Fe(OH)2 . 所以答案是:①2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑,钠元素;②碳、氧,熟石灰;③FeCl2(或其他亚铁盐).
2NaOH+H2↑+Cl2↑,钠元素;②碳、氧,熟石灰;③FeCl2(或其他亚铁盐).
【考点精析】利用金属材料的选择依据和质量守恒定律及其应用对题目进行判断即可得到答案,需要熟知黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属;①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏.

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案