题目内容
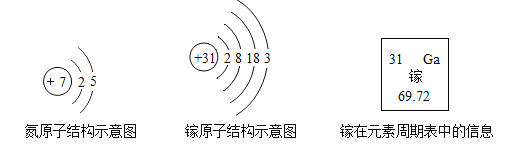
【题目】我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称 LED)技术,已广泛用于照明、显像等多个领域。氮和镓的原子结构示意图及镓在元素周期表中的信息如图所示,下列说法正确的是( )
A.氮元素位于第三周期,属于非金属元素
B.镓原子核内有31个中子
C.镓的相对原子质量是69.72g
D.氮化镓的化学式为GaN
【答案】D
【解析】
A、电子层数决定周期数,氮原子核外有2层,则位于第二周期,镓元素带有钅字旁,属于金属元素,故A错误;
B、左上角属于原子序数等于核内质子数等于核电荷数,中子数≈相对原子质量-质子数,带入计算并不等于31,故B错误;
C、相对原子质量单位是“1”,常省略不写,而选项当中带了g,故C错误;
D、镓的最外层电子数是3易失3个电子,显+3价,氮最外层5个电子易得3个电子,显3价,所以氮化镓表示GaN,故D正确。
故选D。

练习册系列答案
相关题目