题目内容
【题目】无机非金属材料中,用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下:
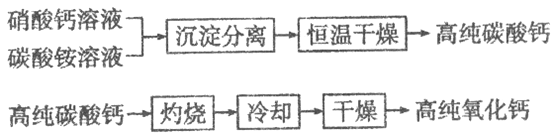
请回答下列问题:
(1)硝酸钙与碳酸铵在溶液中反应,其基本反应类型为___________。
(2)高纯氧化钙生产过程中,“干燥”的主要目的是为了防止__________________ (用化学方程式表示)。
(3)生产高纯碳酸钙时,选择“220℃恒温干燥”而不选择“灼烧”的原因是_______。
【答案】 复分解反应 CaO+H2O=Ca(OH)2 高温灼烧会使碳酸钙分解使所得的碳酸钙中含有氧化钙而不纯
【解析】(1)硝酸钙与碳酸铵在溶液中反应,对应的产物为碳酸钙和硝酸铵,为两种化合物相互交换成分生成两种新的化合物,为复分解反应;
(2)高纯氧化钙生产过程中,由于氧化钙很容易和水反应生成氢氧化钙,所以生成氧化钙的过程中要进行干燥,所以“干燥”的主要目的是为了防止 CaO+H2O=Ca(OH)2;
(3)生产高纯碳酸钙时,选择“220℃恒温干燥”而不选择“灼烧”由于高温时碳酸钙能够分解产生氧化钙,而导致碳酸钙中混有氧化钙。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】我市石灰石资源丰富,某课外小组同学为了测定石灰石中碳酸钙的质量分数,取某地石灰石样品10.0g于烧杯中,将100g稀盐酸分5次加入烧杯中,充分反应后(杂质不与稀盐酸反应),测得剩余固体的质量记录如下.
次数 | 1 | 2 | 3 | 4 | 5 |
加入稀盐酸质量/g | 20 | 20 | 20 | 20 | 20 |
剩余固体质量/g | 8.0 | 6.0 | 4.0 | 2.5 | X |
请计算:(1)X的值为__________.
(2)该石灰石样品中碳酸钙的质量分数为_____________
(3)所用稀盐酸溶质的质量分数为________.(写出计算过程)