题目内容
【题目】分类、类比是学习化学常用的方法。
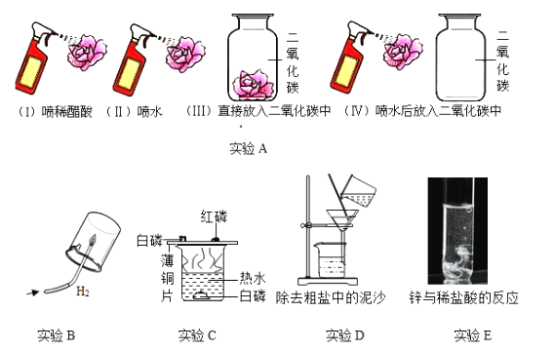
(1)初中化学实验可以按照实验目的分为:“混合物的分离提纯实验”、“探究反应条件实验”“探究物质性质实验”等。据此我们可以将实验A与实验①_____(填字母)分为一类,分类依据是②_____。
(2)在金属活动性顺序中,排在前面的“钾、钙、钠”三种金属与盐溶液接触时先与溶液中的水反应生成碱和氢气。已知金属钾与水反应的化学方程式为:2K+2H2O═2KOH+H2↑.现将金属钠加入硫酸铜溶液中,请写出发生总反应的化学方程式为①_____。金属钠很容易被空气中的氧气氧化,由此推测实验室保存金属钠的注意事项是②_____。
【答案】BE 都是探究物质化学性质的实验 2Na+2H2O+CuSO4═Na2SO4+Cu(OH)2↓+H2↑ 与水和空气隔绝
【解析】
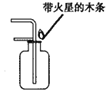
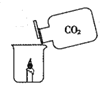
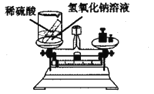
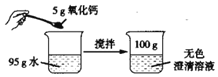
解:(1)A实验是通过颜色变体探究物质的化学性质;B实验是探究氢气的可燃性性质;C实验是探究燃烧的条件;D实验是过滤实验操作;E实验是根据锌与盐酸的反应来探究锌的化学性质;由此可知,B和E两个实验都与A实验相似,都是探究物质化学性质的实验;
故填:BE;都是探究物质化学性质的实验;
(2)由题目信息可知,“钾、钙、钠”三种金属与盐溶液接触时先与溶液中的水反应生成碱和氢气,然后再与盐反应,故将金属钠加入硫酸铜溶液中,反应物有钠、水、硫酸铜,生成物是氢氧化铜、硫酸钠和氢气;发生总反应的化学方程式为:2Na+2H2O+CuSO4═Na2SO4+Cu(OH)2↓+H2↑;金属钠能与水反应,且很容易被空气中的氧气氧化,由此推测实验室保存金属钠的注意事项应该是使钠与水和空气隔绝;
故填:2Na+2H2O+CuSO4═Na2SO4+Cu(OH)2↓+H2↑;与水和空气隔绝。

【题目】某同学为了测定生铁样品中铁的质量分数,将60g 稀盐酸分3次加入到盛有4g 该样品的烧杯中(样品中只有铁与稀盐酸反应),所得数据如表,则下列说法中正确的是( )
实验次数 物质质量 | 第1次 | 第2次 | 第3次 |
加入稀盐酸的质量/g | 20 | 20 | 20 |
充分反应后剩余固体的质量 | 2.6 | 1.2 | 0.1 |
A. 第1次和第2次产生氢气的质量不同
B. 第2次和第3次剩余固体中均有铁
C. 第3次充分反应后溶液中溶质只有FeCl2
D. 生铁样品中铁的质量分数为97.5%
【题目】下表是KNO3、NaCl在不同温度下的溶解度。
温度(℃) | 0 | 20 | 30 | 40 | 60 | 80 | |
溶解度 | KNO3 | 13.3 | 31.6 | 45.8 | 63.9 | 110 | 169 |
NaCl | 35.7 | 36.0 | 36.3 | 36.6 | 37.3 | 38.4 | |
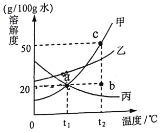
(1)根据表中的数据,在坐标纸上绘制出氯化钠和硝酸钾两种物质的溶解度曲线。(在答题卡的坐标纸上绘图)____
①两种物质中,溶解度受温度的影响变化较大的是_____。
②根据绘制的溶解度曲线可知,50℃时,硝酸钾的溶解度约为_____。
③将接近饱和的KNO3溶液转化为饱和溶液的一种方法是_____。
④从较浓的NaCl溶液中得到NaCl晶体,较好的方法是_____(填“蒸发结晶”或“降温结晶”)。
(2)A是80℃含有120g水的KNO3溶液,经过如下操作,得到102gKNO3固体。
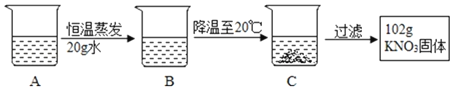
①A溶液为_____(选填“饱和”或“不饱和”)溶液。
②对以上过程的分析,正确的是_____(选填编号)。
a.A到B的过程中,溶质质量没有改变
b.B中溶质与溶剂的质量比为169:100
c.开始析出KNO3固体的温度在60℃至80℃之间
d.A溶液的质量等于222g
(3)烧杯内原有某物质,向其中加入物质X,X的质量与变量Y的关系如图,下列一定能正确反映X、Y对应关系的是_____。
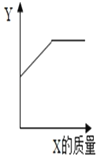
选项 | 烧杯内原有物质 | X | Y |
A | NaCl饱和溶液 | NaCl固体 | NaCl溶液的溶质质量分数 |
B | 水 | NH4NO3固体 | 溶液的温度 |
C | 氯化亚铁溶液 | 锌粉 | 溶液的质量 |
D | 稀硫酸 | 铁粉 | 溶液中氢元素的质量 |