题目内容
【题目】往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续地加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法不正确的是
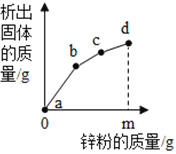
A.c点对应溶液中含有的金属离子为Zn2+和Cu2+
B.bc段(不含两个端点)析出的金属是Cu
C.ab段(不含两个端点)对应溶液中含有的金属离子为Zn2+、Ag+、Cu2+和Fe2+
D.若bc段和cd段中析出固体质量相等,则前后两段参加反应的锌粉质量比为7:8
【答案】A
【解析】
往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续地加入质量为m的锌粉,反应顺序是先弱后强,就是先与活性较弱的金属的化合物反应,再与活动性较强的金属的化合物反应。
A、c点对应溶液是锌刚好与硝酸铜反应完,溶液中含有的金属离子为Zn2+和Fe2+,没有Cu2+,符合题意;
B、bc段(不含两个端点)表示锌与硝酸铜反应,析出的金属是Cu,不符合题意;
C、ab段(不含两个端点)表示锌与硝酸银反应,且没有反应完,因此对应溶液中含有的金属离子为Zn2+、Ag+、Cu2+和Fe2+,不符合题意;
D、若bc段和cd段中析出固体质量相等。
解:设bc段或cd段中析出固体质量为M;bc段参加反应的锌粉质量为X;cd段参加反应的锌粉质量为Y。
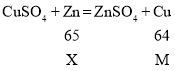
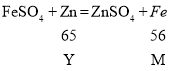
![]()
![]()
![]()
![]()
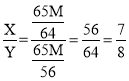 ,不符合题意。故选A。
,不符合题意。故选A。

【题目】某化学兴趣小组为了测定粗锌中锌的质量分数,在10g粗锌中分5次共加入50.0g稀硫酸(杂质不与硫酸反应),部分数据如下表所示,请计算:
容器中硫酸的质量/g | 10 | 20 | 40 | 50 |
气体质量/g | 0.1 | 0.2 | m | 0.3 |
(1)当加入40g硫酸时,对应的气体质量m是___________g。
(2)粗锌中锌的质量_______________________。
【题目】某碳酸钙样品中含有不和盐酸反应的杂质。某同学取12g该样品于烧杯中,再向烧杯中将100g稀盐酸分五次加入样品中,充分反应使气体全部逸出后,称得烧杯中所盛物质的总质量(不包含烧杯自身质量)如下表所示:
实验序号 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
烧杯中所盛物质的总质量/g | 30.90 | 49.80 | m | 87.60 | 107.05 |
请填空:
(1)碳酸钙和盐酸反应的化学方程式为_____;
(2)m的值为_____g;。
(3)12g石灰石样品中碳酸钙的质量分数等于_____;
(4)求反应完全后,溶液中氯化钙的质量_____(写计算过程,保留两位小数)。
【题目】某兴趣小组对KCIO3分解反应的催化剂进行研究,在相同的加热条件下,用如图装置完成表中实验:
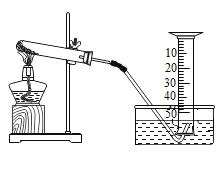
编号 | KCIO3质量/g | 催化剂 | 催化剂质量/g | 收集50 mLO2所需时间/s |
实验1 | 5 | 一 | 一 | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
(1)设置实验1的目的是_____________。
(2)表中所列3种催化剂的催化效果最佳的是___________________。
(3)写出KCIO3分解的化学方程式:________________。
(4)由实验1和实验4可知,KC1_______________ (填“有"或“无”)催化作用。
(5)要比较KCIO3分解反应中不同催化剂的催化效果,除了测量收集50 mLO3所需时间外,还可以测量相同时间内______________。