题目内容
【题目】某化学兴趣小组为了测定粗锌中锌的质量分数,在10g粗锌中分5次共加入50.0g稀硫酸(杂质不与硫酸反应),部分数据如下表所示,请计算:
容器中硫酸的质量/g | 10 | 20 | 40 | 50 |
气体质量/g | 0.1 | 0.2 | m | 0.3 |
(1)当加入40g硫酸时,对应的气体质量m是___________g。
(2)粗锌中锌的质量_______________________。
【答案】0.3 9.75g
【解析】
(1)由表格数据分析可知,每次加入10g稀硫酸,完全反应能产生0.1g氢气,加入50g稀硫酸,若能完全反应,产生的氢气质量应为0.5g,而实际上产生的氢气的质量为0.3g,说明加入30g稀硫酸时,恰好完全反应;则加入40g稀硫酸,稀硫酸有剩余,则对应的气体质量m是0.3g。
(2)设粗锌中锌的质量为x
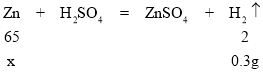
![]()
解得:x=9.75g
答:粗锌中锌的质量为9.75g。

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目