题目内容
【题目】现有Ca(OH)2、CaCO3和一些杂质(不与稀盐酸反应)组成的混合物共15g,取某浓度的稀盐酸,逐滴滴加到混合物中,充分反应,测得稀盐酸的质量与反应生成气体的质量,关系如图所示:
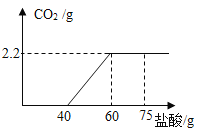
(1)生成CO2的质量是_______g;
(2)计算混合物中CaCO3的质量分数 (写出计算过程,结果精确到0.1%)_____;
(3)所取稀盐酸的浓度是______,欲配制100g该浓度的稀盐酸,需要溶质质量分数为36.5%的盐酸_______g。
【答案】(1)2.2;(2)33.3%;(3)18.25%;50
【解析】
(1)由图可知,生成二氧化碳的质量为2.2g,故填2.2。
(2)解:设参加反应的CaCO3的质量为x。
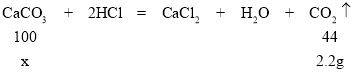
![]()
x=5g
混合物中CaCO3的质量分数为:![]() ×100%≈33.3%
×100%≈33.3%
答:混合物中CaCO3的质量分数为33.3%。
(3)解:设参加反应的纯净HCl的质量为y
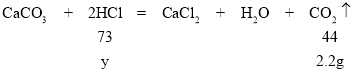
![]()
y=3.65g
由图可知,生成2.2g二氧化碳时,与碳酸钙反应的盐酸的质量为60g40g=20g
所取稀盐酸的浓度为![]() ×100%=18.25%
×100%=18.25%
配制100g该浓度的稀盐酸,需要溶质质量分数为36.5%的盐酸质量为100g×18.25%÷36.5%=50g
答:所取稀盐酸的浓度为18.25%,需要溶质质量分数为36.5%的盐酸质量为50g。

练习册系列答案
相关题目
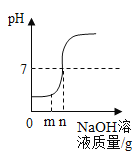
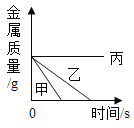
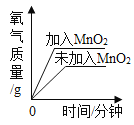
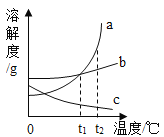
【题目】下列图象中有关的量的变化与对应叙述相符的是( )
A | B | C | D |
|
|
|
|
向盐酸中加入的氢氧化钠溶液为mg时,所得溶液显碱性 | 向三份完全相同的稀盐酸中分别加入甲、乙、丙三种金属,则甲、乙的金属活动性比丙的强 | 用等质量、等浓度的双氧水分别制取氧气 | 将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,所得溶液变成不饱和溶液 |
A.AB.BC.CD.D