题目内容
【题目】著名化学家侯德榜发明了联合制碱法,为我国化学工业的发展做出来杰出贡献.某实验小组取仅含有氯化钠杂质的纯碱样品14.4g,加入到盛有100g稀盐酸的烧杯中,恰好完全反应.此时烧杯内各物质的总质量为110g。试计算:
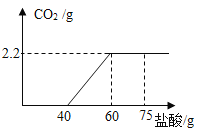
(1)反应生成二氧化碳___________克。
(2)所用稀盐酸的质量分数?
(3)反应后所得溶液中溶质的质量分数?(计算结果精确到0.1%)
【答案】(1) 4.4g;(2) 7.3%;(3) 14.1%
【解析】
(1)由于碳酸钠与稀盐酸的反应放出二氧化碳气体,由质量守恒定律可知,烧杯内物质减少的质量就是生成的二氧化碳的质量为:14.4g+100g-110g=4.4g;
(2)设所用稀盐酸中溶质的质量为x,生成氯化钠的质量为y,原固体混合物中碳酸钠的质量为z,
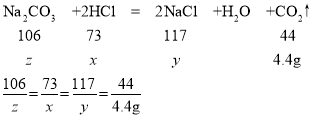
解得:x=7.3g;y=11.7g;z=10.6g
所用稀盐酸的质量分数是:![]() ×100%=7.3%
×100%=7.3%
答:所用稀盐酸的质量分数是7.3%。
(3)所得溶液中溶质的质量=11.7g+(14.4g-10.6g)=15.5g
所得溶液中溶质的质量分数=![]() ×100%≈14.1%;
×100%≈14.1%;
答:溶液中溶质的质量分数是14.1%。

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案【题目】甲同学对寒痛乐熨剂(简称“寒痛乐”)的发热原理产生了浓厚兴趣,于是带了几包寒痛乐,来到实验室对其进行研究。

(查阅资料)
[用法用量] 外用,一日1次。将外袋剪开,取出药袋,晃动数次,使药物充分松散,接触空气,手摸有热感时,置于固定袋内,覆盖于痛患处,每袋可发热不少于15小时。
[原料层] 铁、蛭石、活性炭、水等。
[作用原理] 铁跟氧气和水反应生成氢氧化铁(固体),并放热。
(实验一)验证寒痛乐成分中所含铁的化学性质。
步骤 | 实验操作 | 实验现象 |
① | 将寒痛乐打开,将药物倒入一烧杯中,观察 | 药物为黑色固体粉末 |
② | 用一条形磁铁与烧杯中的黑色粉末充分接触,取适量吸附在磁铁上的黑色粉末放于燃烧匙中,在酒精灯上点燃后伸入盛有氧气的集气瓶中,观察 | 剧烈燃烧,_ |
实验结论:写出此反应的文字表达式_。集气瓶中加水的作用是__。
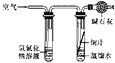
(实验二)用寒痛乐熨剂药粉测定空气中氧气的含量。
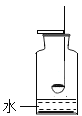
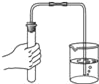
甲同学设计了如图所示装置,进行实验。

(实验记录 )
步骤 | 实验操作 | 主要实验现象 | 实验结论及解释 |
① | 连接好装置如上图所示,然后_____ | _______ | 装置的气密性良好 |
② | 加入足量药品,迅速将胶塞盖严,并充分振荡 | _____ | 进入集气瓶内水的体积即为空气中氧气的含量。 |
(实验反思)乙同学认为甲同学所做“寒痛乐药粉测定空气中氧气的含量”的实验不能证明上述结论,他将操作改进后再进行测量,得到了较为准确的结果。他改进后的操作为____。
【题目】请你参与某学习小组的探究活动,并回答相关问题:
[发现问题]小丽发现盛水的铁锅在与水面接触的部位最易生锈;小茜发现自己的铜
制眼眶表面出现了绿色的铜锈;小玲发现苹果切开不久,果肉上会产生一层咖啡色物质,好像生了“锈”一般.
[提出问题]这三种物质“生锈”的原因是什么?
[收集证据] (1)回忆已有知识:铁生锈的条件是______________________________.
[查阅有关资料]“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿);苹果“生锈”是果肉里的物质(酚和酶)与空气中的氧气发生了一系列的反应,生成咖啡色的物质.碱石灰能吸水.
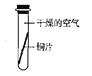
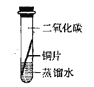
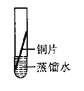
[实验探究]将四小块铜片分别按下图所示放置一个月,观察现象如下:
实验 装置 |
|
|
|
|
实验验象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面附近锈蚀最严重 |
由实验可知,铜生锈是铜与水、__________、_________等物质共同作用的结果.
[得出结论]经过交流讨论,三位同学认为这些物质“生锈”除了可能与水有关外,还可能都与___________________(填物质名称)有关.
[反思与应用] 利用所得结论填空:
(1)写出一种防止铁或铜等金属制品生锈的具体方法_________________________.
(2)请你提出一条延长食品保质期的建议___________________________________.