题目内容
【题目】A~G是初中化学常见的物质,其中A、B、D、E都是氧化物,C、F、G都是金属单质,A为红棕色固体,E为黑色固体,它们之间的转化关系如图所示(部分反应物和生成物已略去)。请回答:
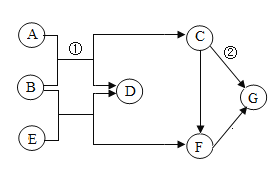
(1)E的化学式为_________。
(2)D的一种用途是_______________。
(3)C、F、G三种金属的活动性由弱到强的顺序为____________。
(4)反应①的化学方程式为__________。反应②的基本反应类型是________。
【答案】CuO 灭火(或气体肥料或光合作用或人工降雨等)(合理均给分) G、F、C(或G<F<C 或G小于F小于C) 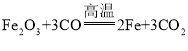 置换反应
置换反应
【解析】
A、B、D、E都是氧化物,C、F、G都是金属单质,A为红棕色固体,则A为氧化铁,E为黑色固体,则E为氧化铜;A、E为金属氧化物,B具有还原性,则B为一氧化碳;氧化铁和一氧化碳反应生成铁和二氧化碳,则D为二氧化碳,C为铁;氧化铜和一氧化碳反应生成铜和二氧化碳,则F为铜;C生成F,铁与硫酸铜反应生成铜和硫酸亚铁;铁和铜都能生成G,则G在金属活动性排在铁和铜的前面,可以为银。通过检验,推测合理。
(1)E为氧化铜,化学式为CuO 。
(2)D是二氧化碳气体,用于灭火。
(3)C能置换F,C比F活泼,C、F分别能置换G,F比G活泼,三种金属的活动性由弱到强的顺序为G<F<C 。
(4)反应①的化学方程式为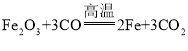 。反应②是金属与盐反应生成另一种金属和另一种盐,属于置换反应。
。反应②是金属与盐反应生成另一种金属和另一种盐,属于置换反应。

【题目】请你参与某学习小组的探究活动,并回答相关问题:
[发现问题]小丽发现盛水的铁锅在与水面接触的部位最易生锈;小茜发现自己的铜
制眼眶表面出现了绿色的铜锈;小玲发现苹果切开不久,果肉上会产生一层咖啡色物质,好像生了“锈”一般.
[提出问题]这三种物质“生锈”的原因是什么?
[收集证据] (1)回忆已有知识:铁生锈的条件是______________________________.
[查阅有关资料]“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿);苹果“生锈”是果肉里的物质(酚和酶)与空气中的氧气发生了一系列的反应,生成咖啡色的物质.碱石灰能吸水.
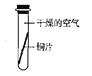
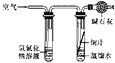
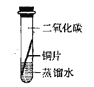
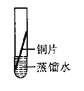
[实验探究]将四小块铜片分别按下图所示放置一个月,观察现象如下:
实验 装置 |
|
|
|
|
实验验象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面附近锈蚀最严重 |
由实验可知,铜生锈是铜与水、__________、_________等物质共同作用的结果.
[得出结论]经过交流讨论,三位同学认为这些物质“生锈”除了可能与水有关外,还可能都与___________________(填物质名称)有关.
[反思与应用] 利用所得结论填空:
(1)写出一种防止铁或铜等金属制品生锈的具体方法_________________________.
(2)请你提出一条延长食品保质期的建议___________________________________.