题目内容
【题目】结合下图仪器,完成粗盐提纯实验中的有关问题。
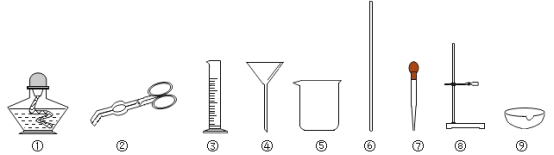
(1)在溶解粗盐时,用到仪器⑥,其作用是____________________________。
(2)蒸发结晶食盐,除用到②⑥⑧⑨,还需用到图中的仪器有______(填序号)。
(3)下列有关蒸发结晶操作描述正确的是______。
a.当加热至有晶体析出时,即停止加热 b.当蒸发皿中出现较多固体时,即停止加热
c.当水分完全蒸干时,即停止加热 d.蒸发皿应放在石棉网上加热,放止破损
【答案】搅拌、加速溶解 ① B
【解析】
(1)在溶解操作中,玻璃棒起到搅拌以加快粗盐的溶解的作用。
(2)固体溶解度随着温度变化不大的物质需蒸发结晶,氯化钠属于该类,所以把所得滤液倒入蒸发皿,用酒精灯加热,待蒸发皿中出现较多固体时,停止加热,利用余热蒸干,所以实验过程中需要用到①酒精灯。
(3)蒸发结晶实验的步骤是:在蒸发皿中进行,蒸发皿放于铁架台的铁圈上,倒入液体不超过蒸发皿容积的![]() ,蒸发过程中不断用玻璃棒搅拌液体,防止受热不均,液体飞溅。看到有大量固体析出,或者仅余少量液体时,停止加热,利用余热将液体蒸干。因此b符合题意。
,蒸发过程中不断用玻璃棒搅拌液体,防止受热不均,液体飞溅。看到有大量固体析出,或者仅余少量液体时,停止加热,利用余热将液体蒸干。因此b符合题意。

【题目】已知:20℃时,a和b的溶解度分别为36g和88g。
| 序号 | ① | ② | ③ | ④ | ⑤ |
|
固体种类 | a | a | b | b | b | ||
固体的质量/g | 30 | 60 | 30 | 60 | 90 | ||
水的质量/g | 100 | 100 | 100 | 100 | 100 |
下列说法不正确的是
A.20℃时,⑤中溶质与溶剂的质量比为88:100
B.将t1℃时b的饱和溶液加水可变为不饱和溶液
C.将t2℃时a的饱和溶液降温至t1℃,溶液质量不变
D.将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等
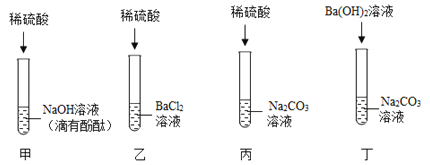
【题目】某校化学兴趣小组在探究“酸碱盐的相关性质”时,做了如图一所示的两个实验,实验结束后,小组同学将两支试管中的废液同时倒入一个洁净的烧杯中(如图所示),观察到有气泡产生,为确认烧杯内溶液中溶质的成分,同学们进行了如下探究。

(查阅资料)Na2SO4溶液、NaCl溶液呈中性。
(提出猜想)猜想1:Na2SO4、NaCl;猜想2:Na2SO4、NaCl和________;猜想3:Na2SO4、NaCl和H2SO4;猜想4:Na2SO4、NaCl、H2SO4和Na2CO3。
(交流讨论)小强同学认为猜想4一定是错误的,他的理由是______(用化学方程式表示)。
(进行实验)小明同学设计如下两个实验方案:
实验步骤 | 实验现象 | 实验结论 | |
方案一 | 取少量烧杯中的溶液于洁净的试管中,加入一定量氧化铜固体 | ______ | 猜想3正确 |
方案二 | 取少量烧杯中的溶液于洁净的试管中,加入适量的硝酸钡溶液 | 产生白色沉淀 |
请写出方案一中有关反应的化学方程式:________。
(反思与总结)(1)有同学认为方案二不合理,分析原因_________。
(2)分析反应后溶液中溶质成分,除要考虑生成物外,还需考虑反应物是否过量。
【题目】下表是 20℃时部分物质的溶解度数据。
物质 | Ca(OH)2 | NaOH | CaCO3 | Ca(HCO3)2 | Na2CO3 | NaHCO3 |
溶解度/g | 0.16 | 109 | 0.0065 | 16.6 | 21.8 | 9.6 |
(1)配制溶液:配制 50g11%氢氧化钠溶液的基本步骤是:计算—称取氢氧化钠固体—量取水—溶解—装瓶贴标签。 用托盘天平称取氢氧化钠固体的质量_________ g。
(2)进行性质探究实验,20℃时,根据数据回答下列问题:
①向稀氢氧化钠溶液中通入 CO2,先生成 Na2CO3,继续通入 CO2,Na2CO3 会转化为 NaHCO3,已知后者为化合反应,请写出该化合反应的化学方程式:_________。 若向 20℃时饱和 Na2CO3 溶液中通入过量的 CO2,可观察到的现象是_________。
②结合表格中的有关数据,若以 20℃时,100g 饱和溶液吸收 CO2 的质量最大为依据,则除去 CO 气体中的 CO2 杂质,应选择_________溶液(填化学式),欲检验CO2气体的存在,则应选择_________溶液(填化学式)。
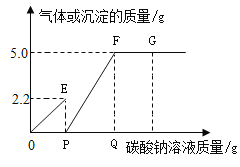
③将 2.2g CO2 通入 47.8g 一定浓度的 NaOH溶液中充分反应后(反应过程中没有CO2 逸出,水也没有蒸发),溶液中的溶质仅有 Na2CO3和 NaHCO3 两种物质(NaHCO3 在水中电离成 Na+和 HCO3-),则此时溶液中碳元素的质量分数为__________,在此反应过程中,你认为钠离子的个数_________发生变化?(填写: 有或者没有)
(3)电导率传感器可辅助探究复分解反应的实质。相同条件下,离子浓度越大,电导率越大,溶液导电性越强。将含有酚酞的 Ba(OH)2 溶液平均分成两份置于两个烧杯中 并插入电导率传感器,往其中一份滴加稀硫酸,往另一份滴加硫酸钠溶液,滴加过程中,这两份溶液的滴加速率始终相同,测得溶液的电导率变化如图所示。下列说法正确的是__________
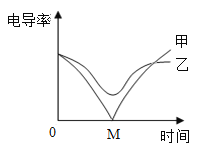
a.乙曲线电导率减小过程中,溶液由红色变为无色
b.乙曲线对应的反应中四种离子数目都减少
c.甲曲线对应氢氧化钡与硫酸钠反应
d.甲曲线上的 M 点代表两种溶液恰好完全反应