题目内容
【题目】如图所示的是物质A~G相互间的关系(“→”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应)A、F都是单质;F是使用最多的金属材料;B是导致温室效应的主要气体;在工业上,C广泛用于玻璃、造纸、纺织和洗涤剂的生产等;D的一种俗名为消石灰;E是一种蓝色溶液。请回答:
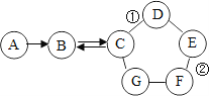
(1)C的化学式______,G可能是______(写名称)。
(2)写出D的一种重要用途______。(合理即可)
(3)写出标号①、②的化学反应方程式①______②______,反应的类型属于______。
【答案】Na2CO3 盐酸或硫酸 改良酸性土壤 Na2CO3+Ca(OH)2=2NaOH+CaCO3↓ Fe+CuSO4=FeSO4+Cu 置换反应
【解析】
(1)A、F都是单质,F是使用最多的金属材料,所以F是铁,B是导致温室效应的主要气体,所以B是二氧化碳,在工业上,C广泛用于玻璃、造纸、纺织和洗涤剂的生产等,所以C是碳酸钠,E是一种蓝色溶液,所以E中含有铜离子,由图示可知A可能是碳或氧气,G能够与碳酸钠和铁反应,所以G是酸可以是盐酸或硫酸,D的一种俗名为消石灰,所以D是氢氧化钙,经过验证,推导正确,所以C的化学式Na2CO3,G可能是盐酸或硫酸;
(2)D的一种重要用途是改良酸性土壤;
(3)反应①是碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
反应②是铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu,该反应的类型属于置换反应。
故答案为:(1)Na2CO3,盐酸或硫酸;
(2)改良酸性土壤;
(3)Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
Fe+CuSO4=FeSO4+Cu,置换反应。

【题目】老师在分析金属和盐溶液反应时指出在金属活动性的顺序里,位于前面的金属能把排在后面的金属从它们的盐溶液中置换出来,但钾、钙、钠除外。李明同学很好奇,于是做了钠与硫酸铜溶液反应的实验。
(进行试验)
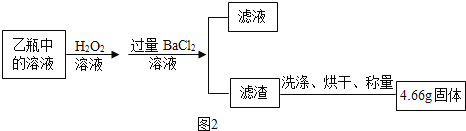
一块4.6g的金属钠,放入盛有一定量硫酸铜溶液的烧杯中,发现金属钠浮在液面上不停打转,产生大量气体,烧杯发烫,溶液中出现了蓝色絮状沉淀,并没有出现紫红色的铜,一会儿,部分沉淀逐渐变黑。充分反应后,冷却过滤,得到滤液是无色。
(提出问题)
金属钠与硫酸铜溶液反应后的产物是什么?无色滤液的成分是什么?
(查阅资料)
(1)①钠能与水反应生成一种碱,同时放出气体。
②氢氧化铜受热至60℃ ~80℃变暗,温度过高时分解为相应的金属氧化物和水。
(实验探究1)探究生成的气体是什么?
李明同学将上述实验药品放入锥形瓶中,立即塞上带导管的单孔塞,将导管通入肥皂水中,将燃着的木条靠近飘起的肥皂泡,有爆鸣声。说明生成的气体是____________。
(实验探究2)探究沉淀的成分是什么?
(猜想与假设)沉淀中有Cu(OH)2和CuO,还可能含有Cu。
(实验验证)
实验步骤 | 实验现象 | 结论 |
将锥形瓶内反应后过滤所得滤渣放入烧杯内,并加入足量的______ | _________ | 沉淀中没有Cu |
(实验结论)
通过实验,李明同学得出结论:钠加入硫酸铜溶液会先与水反应,生成的碱再与硫酸铜反应生成氢氧化铜。写出生成的碱与硫酸铜反应的化学方程式______________。
(实验探究3)滤液的成分是什么?
通过分析,李明同学得出:所得的无色滤液中一定含有硫酸钠,还可能含有______________。
若要证明是否含有该物质,只需向无色滤液中滴加______________ (填物质名称)观察现象即可获得结论。
(反思与交流)
(1)出现黑色物质的可能原因是______________。
(2)设计一个简单实验证明硫酸铜溶液显蓝色是由Cu2+引起的。你的方案是______________。(要求写出实验步骤和现象)
(3)钠完全反成后,所得无色滤液中硫酸钠的质量若用a表示,则a的取值范围是______________。
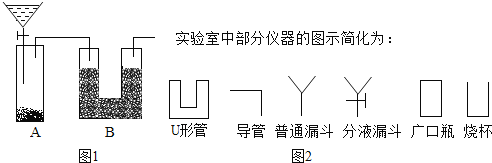
【题目】某班同学为检验氢氧化钠溶液是否变质,向盛有氢氧化钠溶液的试管中加入一定量的稀盐酸,迅速用带导气管的橡胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的 试管中观察到澄清石灰水变浑浊(如图所示)。请回答下列问题(提示:CaCl2溶液显中性):
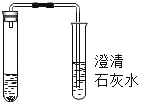
(1)氢氧化钠溶液变质的化学反应化学方程式为_____。
(2)实验结束后,将两支试管中的所有物质倒入同一个废液缸中, 充分反应后得到澄清溶液。同学们对废液中溶质的成分进行如下探究(忽略二氧化碳的影响):
(提出问题)废液中溶质的成分是什么?
(做出猜想)
猜想一:CaCl2、NaCl和HCl
猜想二:CaCl2、NaCl和Na2CO3
猜想三:CaCl2、NaCl
小明对上述猜想二提出质疑,认为该猜想不成立。其原因是_____。
(设计实验)请完成实验报告
实验步骤 | 实验现象 | 实验结论 |
取少量废液于试管中,加入_____; | _____ | 猜想一成立 |
(反思拓展)最终同学们确认了废液中溶质的成分。若将废液直接排入铸铁管道引起的危害是_____,你认为该废液的处理方法是_____。
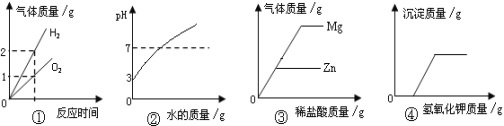
向含有氯化钠、氯化钙和稀盐酸的混合溶液中滴加碳酸钠溶液, 溶液的 pH变化情况如图所示:
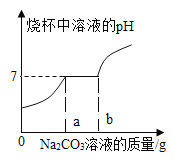
(1)0-a段发生的化学反应方程式为_____。
(2)a-b 段溶液的 pH 没有变化的原因是:_____。