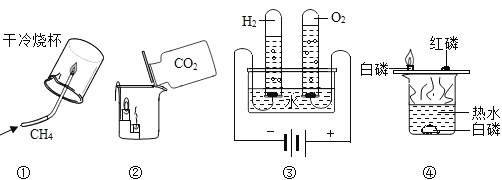
题目内容
【题目】某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。请计算:
(1)若要清洗1000kg的这种石油产品,需要______kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。每处理1000kg这种产品,可以节约多少经费?已知工业级的NaOH和Ca(OH)2的最新市场批发价如下表:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 1.00 | 6.00 |
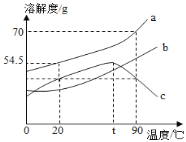
(3)请画出用氢氧化钠和氢氧化钙处理1000kg该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线表示,氢氧化钙用实线表示。______
(4)将反应后生成的硫酸钙回收,在一定条件下加入高温硫酸盐还原菌,可以将SO42-离子转化生成H2S气体,然后用以硫酸的生产工业。不考虑整个过程中硫元素的损失,若将(2)中产生的硫酸钙全部转化,可生产H2S的质量为______kg。
【答案】40  17
17
【解析】
(1)设需要氢氧化钠的质量为x

x=40kg
故填:40;
(2)设需要用Ca(OH)2的质量为y

![]()
y=37kg
氢氧化钠需要的费用为:
6元/kg×40kg=240元;
氢氧化钙需要的费用为:
1元/kg×37kg=37元
可以节约的费用为:240元-37元=203元;
答:可以节约的费用为203元;
(3)最开始硫酸的量为1000kg×4.9%=49kg,消耗氢氧化钙的质量为37kg,氢氧化钠的质量为40kg,故填:

(4)设产生硫化氢的质量为z

z=17kg
故填:17。

【题目】兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质利用数字化传感器测得烧杯中溶液pH的变化图象进行相关探究。
(提出问题)它们溶液的酸碱性及与酸反应时溶液的pH如何变化?
(实验探究1)向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 | 蒸馏水 | 碳酸氢钠溶液(A) | 碳酸钠溶液(B) | 氢氧化钠溶液(C) |
紫甘蓝汁液显示的颜色 | 蓝紫色 | 蓝色 | 绿色 | 黄色 |
查阅资料:
pH | 7.5~9 | 10~11.9 | 12~14 |
紫甘蓝汁液显示的颜色 | 蓝色 | 绿色 | 黄色 |
(得出结论1)三种溶液的碱性由强到弱的顺序为______。(用A、B、C表示)
(实验探究2)甲同学在烧杯溶液中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液由_____色变为____色。向其中加入稀盐酸,该反应的化学方程式为______。
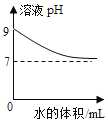
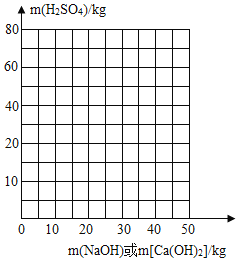
乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如下图所示.
(得出结论2)①从微观角度分析,该反应的实质是____。
②如图所示,下列说法正确的是(___________)
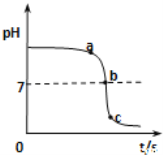
A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是只有NaCl
C.该实验是将氢氧化钠溶液逐滴滴入到盛有盐酸的烧杯中
D.由a点到b点的pH变化过程证明酸和碱发生了中和反应