题目内容
【题目】下图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。
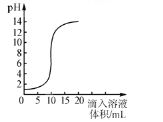
下列说法不正确的是
A.该实验是将氢氧化钠溶液滴入盐酸中
B.氢氧化钠溶液和盐酸恰好反应时,溶液PH=7
C.当滴加入20ml溶液时,再滴加石蕊试剂,溶液呈红色
D.当PH=12时,所得溶液的溶质为NaCl和NaOH
【答案】C
【解析】
试题分析:A、根据图示可知,该实验是将氢氧化钠溶液滴入盐酸中,正确;B、氢氧化钠溶液和盐酸恰好反应时,溶液PH=7,正确;C、当滴加入20ml溶液时,溶液呈碱性,说明氢氧化钠溶液过量,盐酸已完全消耗,再滴加石蕊试剂,氢氧化钠溶液使石蕊试剂变为蓝色,错误;D、当PH=12时,说明盐酸完全消耗,氢氧化钠溶液过量,则所得溶液的溶质为NaCl和NaOH,正确。故选C

【题目】实验室有一瓶长期露置于空气中氢氧化钠溶液,确认已变质。某学习小组展开如下探究,确定该溶液的成分,并进一步制定回收方案。
【问题1】久置的氢氧化钠溶液是全部变质?还是部分变质?
【探究1】确定该溶液中溶质的成分。
【资料1】BaCl2溶液、Ba(NO3)2溶液、CaCl2溶液、Ca(NO3)2溶液、NaNO3溶液均显中性。
实验操作 | 实验现象 | 实验结论 |
Ⅰ.取少量溶液于试管中,向溶液中滴加 (14) 溶液,并不断振荡。 | 白色沉淀产生 | 该溶液部分变质,含有 碳酸钠和氢氧化钠。 |
Ⅱ.将步骤Ⅰ反应后的混合物静置,取少量上层清液,滴加2~3滴酚酞试液。 | (15) |
氢氧化钠溶液变质的原因 (16) (用化学方程式表示),因此氢氧化钠溶液必须密封保存。
【问题2】如何从变质的氢氧化钠溶液中回收得到较纯净的氢氧化钠固体。
【探究2】回收纯净的氢氧化钠固体。
【资料2】在不同温度下NaOH的溶解度如下:
温度(℃) | 10 | 20 | 40 | 60 | 80 | 100 |
溶解度(g/100g水) | 64 | 85 | 138 | 203 | 285 | 376 |
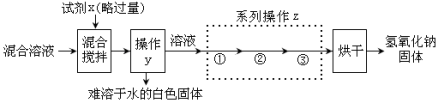
请回答下列问题:
Ⅰ.试剂x的化学式 (17) ,操作y的名称为 (18) 。
Ⅱ.根据相关物质的溶解度数据,系列操作z中 ② 操作名称为 (19) 。
Ⅲ.探究1中的物质检验和探究2中的除杂提纯都将碳酸钠进行了转化,但二者目的不同,分别是 (20) 、 (21) 。