题目内容
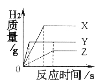
【题目】将相同体积、相同溶质质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如右图所示。下列说法中正确的是
A.三种金属的活动性顺序为X>Z>Y
B.产生氢气的速率顺序为 X>Y>Z
C.反应完成时消耗稀盐酸的质量顺序为X>Y>Z
D.相对原子质量由大到小的顺序为 X>Y>Z
【答案】C
【解析】
试题分析:A、由生成H2的质量与反应时间的关系图可知,在三种金属与稀盐酸进行反应时,相同时间内放出氢气的从多到少的顺序为Y>X>Z,可判断三种金属的活动性顺序为Y>X>Z;故A不正确; B、由三种金属的活动性顺序为Y>X>Z,可判断产生氢气的速率顺序应为Y>X>Z,而非X>Y>Z;故B不正确; C、由生成H2的质量与反应时间的关系图可知,三种金属完全反应放出氢气的质量由大到小的顺序为X>Y>Z,则消耗稀盐酸的质量顺序为X>Y>Z,故正确D、由生成H2的质量与反应时间的关系图可知,三种等质量的金属完全反应放出氢气的质量由大到小的顺序为X>Y>Z,根据一定量金属完全反应产生氢气质量=![]() ×金属的质量,已知三种金属的质量和化合价相同,所以三种金属的相对原子质量关系应为Z>Y>X;故D错误;故答案选择C
×金属的质量,已知三种金属的质量和化合价相同,所以三种金属的相对原子质量关系应为Z>Y>X;故D错误;故答案选择C

【题目】有一种石灰石样品,其中含有的杂质是二氧化硅(它是一种不溶于水,也不与盐酸反应,耐高温的固体物质),某同学想测定该样品的纯度,他取用2 g这种石灰石样品,把20 g稀盐酸分四次加入,充分反应后剩余固体的质量如下表所示:
稀盐酸的质量 | 剩余固体的质量 |
第一次加入5 g | 1.315 g |
第二次加入5 g | 0.63 g |
第三次加入5 g | 0.3 g |
第四次加入5 g | 0.3 g |
(1)2 g石灰石样品中的杂质质量是 g;
(2)石灰石样品的纯度为 ;
(3)100 kg这种纯度的石灰石充分煅烧后,可得到固体多少千克?
【题目】(6分)一定条件下,某物质溶解于水的实验数据如下表,请回答有关问题。
实验序号 | 温度/℃ | 水的质量/g | 所加物质质量/g | 溶液质量/g |
① | 20 | 10 | 2 | 12 |
② | 20 | 15 | 2.5 | a |
③ | 20 | 20 | 7 | 26 |
④ | 30 | 20 | 7 | 27 |
(1)表中a= 。
(2)20℃时,该物质的溶解度为 。
(3)下图中,能表示该物质溶解度的曲线是 (填字母)。
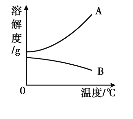
(4)所得溶液一定为饱和溶液的是 (填实验序号,下同);所得溶液中溶质质量分数最大的是 。
(5)温度不变,将①、②所得溶液混合后,向其中再加入 g该物质,能使溶液恰好达到饱和。